
Wetenschap
Formaldehyde-koolstofhybridisatie:een gedetailleerde uitleg
1. De structuur van formaldehyde
Formaldehyde heeft een centraal koolstofatoom dat dubbel gebonden is aan een zuurstofatoom en enkelvoudig gebonden aan twee waterstofatomen. De Lewis-structuur ziet er als volgt uit:
H
|
C =O
|
H
2. Hybridisatie
* Valentie-elektronen van koolstof: Koolstof heeft vier valentie-elektronen (2s² 2p²)
* Hybridisatie: Om de bindingen in formaldehyde te vormen, ondergaat koolstof sp²-hybridisatie . Dit betekent:
* Eén 2s-orbitaal en twee 2p-orbitalen vormen samen drie sp² hybride orbitalen . Deze hybride orbitalen zijn gerangschikt in een trigonale vlakke geometrie, met verbindingshoeken van ongeveer 120 °.
* De resterende 2p-orbitaal op koolstof blijft ongehybridiseerd.
3. Bondvorming
* Sigma-obligaties:
* Twee van de sp² hybride orbitalen op koolstof vormen sigma (σ) bindingen met de 1s orbitalen van de twee waterstofatomen.
* Eén van de sp² hybride orbitalen op koolstof vormt een sigma (σ) binding met de 2p-orbitaal van het zuurstofatoom.
* Pi Bond:
* De ongehybridiseerde 2p-orbitaal op koolstof overlapt met een ongehybridiseerde 2p-orbitaal op zuurstof om een pi (π)-binding te vormen. Deze pi-binding is verantwoordelijk voor de dubbele binding tussen koolstof en zuurstof.
4. Samenvatting
Samenvattend wordt het koolstofatoom in formaldehyde sp² gehybridiseerd, wat resulteert in:
* Drie sp² hybride orbitalen: Vorm sigmabindingen met de twee waterstofatomen en het zuurstofatoom.
* Eén ongehybridiseerde 2p-orbitaal: Vormt een pi-binding met het zuurstofatoom.
Deze hybridisatie en bindingsvorming geven formaldehyde een vlakke geometrie met bindingshoeken van bijna 120°.
 Berekening van de ruwe geboortecijfer
Berekening van de ruwe geboortecijfer Elektriciteit komt niet vaak voor in de natuur behalve de vorm van?
Elektriciteit komt niet vaak voor in de natuur behalve de vorm van?  Wat zijn de symbiotische relaties in een ecosysteem?
Wat zijn de symbiotische relaties in een ecosysteem?  Amerikaanse rechter verwerpt rechtszaken over klimaatverandering tegen grote olie
Amerikaanse rechter verwerpt rechtszaken over klimaatverandering tegen grote olie Zouten liefde voor water kan een sleutelrol spelen bij veilige CO2-opslag
Zouten liefde voor water kan een sleutelrol spelen bij veilige CO2-opslag
Hoofdlijnen
- Welke organel is een niet -gembranous organelle?
- Waar zijn de vrienden van Facebook? Aandelendaling wordt dieper (update)
- Wat geloofden de meeste mensen over genetica vóór Gregor Mendel en onderzoek?
- Waarom is water een biomolecuul?
- Structuur die elk chromosoom op zijn exacte kopie houdt?
- Waarom moet water aanwezig zijn voor de bryophytes om het seksuele deel van de levenscyclus te voltooien?
- Hoe reproduceert een gametophyte zich?
- Het effect van zonlicht op dieren en planten
- Kleine rode dieren schieten in het donker onder het ijs van een bevroren meer in Quebec
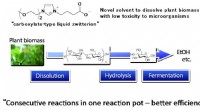
- Nieuw oplosmiddel draagt bij aan de volgende generatie biobrandstofproductie uit biomassa
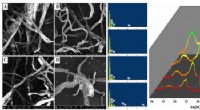
- Wetenschappers rapporteren efficiënt gebruik van oud papier voor de productie van cellulase door Trichoderma longiflorum
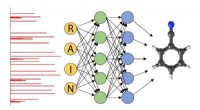
- De volgende fase:neurale netwerken gebruiken om gasfasemoleculen te identificeren
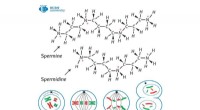
- Biochemicus ontdekt veelbelovend enzym om kankercellen te bestrijden
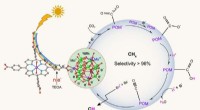
- Op polyoxometalaat gebaseerde coördinatiekaders voor de vorming van methaan bij de fotoreductie van koolstofdioxide
 Is waterstofperoxide een mengsel of pure stof?
Is waterstofperoxide een mengsel of pure stof?  Nieuwe kolenregelgeving zal tot 1400 Amerikanen per jaar doden
Nieuwe kolenregelgeving zal tot 1400 Amerikanen per jaar doden Wat heeft cellulaire ademhaling te maken met zuurstof?
Wat heeft cellulaire ademhaling te maken met zuurstof?  Welke celfunctie wordt onderhouden door deling?
Welke celfunctie wordt onderhouden door deling?  Palladium-gouden nanodeeltjes reinigen TCE een miljard keer sneller dan ijzervijlsel
Palladium-gouden nanodeeltjes reinigen TCE een miljard keer sneller dan ijzervijlsel Wat is de onderste zone van een bodemhorizon?
Wat is de onderste zone van een bodemhorizon?  Zuur-base-neutralisatiereacties:het proces begrijpen
Zuur-base-neutralisatiereacties:het proces begrijpen  Wat zijn twee soorten elektrische circuits?
Wat zijn twee soorten elektrische circuits?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

