
Wetenschap
pH-verandering met sterke zuurtoevoeging:niet-gebufferde oplossingen begrijpen
* Niet-gebufferde oplossingen hebben geen buffersysteem: Buffers zijn oplossingen die bestand zijn tegen veranderingen in de pH wanneer kleine hoeveelheden zuur of base worden toegevoegd. Ze bevatten een zwak zuur en zijn geconjugeerde base (of een zwakke base en zijn geconjugeerde zuur), die toegevoegde H+- of OH--ionen kunnen neutraliseren.
* Sterke zuren dissociëren volledig: Sterke zuren, zoals zoutzuur (HCl) of salpeterzuur (HNO3), ioniseren volledig in oplossing, waarbij een groot aantal waterstofionen (H+) vrijkomt.
* Verhoogde H+-concentratie: De toevoeging van H+-ionen uit het sterke zuur verhoogt direct de concentratie van H+ in de oplossing.
* Lagere pH: pH is een maatstaf voor de zuurgraad of alkaliteit van een oplossing. Een hogere concentratie H+-ionen komt overeen met een lagere pH-waarde, waardoor de oplossing zuurder wordt.
Samengevat: Het toevoegen van zelfs een kleine hoeveelheid sterk zuur aan een niet-gebufferde oplossing verhoogt de H+-concentratie dramatisch, waardoor een aanzienlijke daling van de pH ontstaat.
 Afdrijven van plastic op zee vanuit de ruimte volgen
Afdrijven van plastic op zee vanuit de ruimte volgen Wetenschappers vinden persistente organische verontreinigende stoffen in dierenbont
Wetenschappers vinden persistente organische verontreinigende stoffen in dierenbont NASA's Terra-satelliet vangt einde van Atlantische tropische depressie 15
NASA's Terra-satelliet vangt einde van Atlantische tropische depressie 15 Tol aardbeving Haïti loopt op tot 17
Tol aardbeving Haïti loopt op tot 17 Onderzoek naar de effecten van klimaatverandering op de productie van waterkracht
Onderzoek naar de effecten van klimaatverandering op de productie van waterkracht
Hoofdlijnen
- Wat is de structuur van homeostase?
- Wie was verantwoordelijk voor de celtheorie?
- Hoe libellen zichzelf oprichten als ze ondersteboven worden neergezet
- Wat zijn natuurlijke recorces?
- Wat is waar met betrekking tot bacteriën en dierencellen?
- Wat is de wetenschappelijke naam voor PBO?
- Wat is een verschil tussen onderzoek in het veld en het laboratorium?
- Een universeel raamwerk voor ruimtelijke biologie
- Microben die gaatjes veroorzaken, kunnen superorganismen vormen die kunnen kruipen en zich op de tanden kunnen verspreiden
- Hoe Romeinse cijfers de metaaloxidatietoestanden in chemische verbindingen definiëren

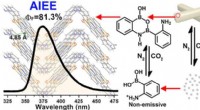
- Nieuw door aggregatie geïnduceerd aromatisch molecuul met verbeterde emissie ontdekt
- Een koolstofvrije wereld katalyseren door energie uit levende cellen te halen
- Een nieuw proces voor volledig gebruik van zachthoutschors

- Een vereenvoudigd nieuw proces zet houtafval uit landbouw en bosbeheer om in ethanol

 Uit onderzoek blijkt waarom veel IVF-embryo's zich niet ontwikkelen
Uit onderzoek blijkt waarom veel IVF-embryo's zich niet ontwikkelen  Racisme, uitsluiting en symbolisme:hoe Māori- en Pacific-afgestudeerden nog steeds worden gemarginaliseerd aan de universiteit
Racisme, uitsluiting en symbolisme:hoe Māori- en Pacific-afgestudeerden nog steeds worden gemarginaliseerd aan de universiteit Kan de invoering van een digitale valuta van de centrale bank de sociale welvaart verbeteren?
Kan de invoering van een digitale valuta van de centrale bank de sociale welvaart verbeteren? Welke kleur heeft de Leo -ster?
Welke kleur heeft de Leo -ster?  Draait een windturbine met de snelheid van het geluid?
Draait een windturbine met de snelheid van het geluid?  Wat zijn de subsets van een lijn in geometrie?
Wat zijn de subsets van een lijn in geometrie?  Kan gewicht worden omgezet in energie?
Kan gewicht worden omgezet in energie?  Soorten mariene groei
Soorten mariene groei
Universeel gesproken zou "mariene groei" verwijzen naar al het leven in de oceaan, inclusief waterplanten, schaaldieren, vissen en in het water levende zoogdieren zoals walvissen. Binnen de scheepvaartindustrie is 'mariene gro
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

