
Wetenschap
Kaliumchloride en water:eigenschappen, interacties en toepassingen
Kaliumchloride (KCl)
* Vast: In zuivere vorm is kaliumchloride een witte kristallijne vaste stof.
* Zout: Het is een ionische verbinding bestaande uit kalium- (K⁺) en chloride- (Cl⁻)-ionen.
* Gebruik: KCl wordt in verschillende toepassingen gebruikt:
* Meststof: Het levert kalium, een essentiële voedingsstof voor de plantengroei.
* Zoutvervanger: Het wordt gebruikt als natriumarm alternatief voor keukenzout.
* Geneeskunde: Het wordt gebruikt in intraveneuze vloeistoffen en als bron van kalium voor medische behandelingen.
* Industrieel: Het wordt gebruikt in verschillende industriële processen, zoals de productie van kunstmest en zeep.
Water (H₂O)
* Vloeistof: Water is bij kamertemperatuur een transparante, smaak- en geurloze vloeistof.
* Oplosmiddel: Het is een zeer effectief oplosmiddel, wat betekent dat het een breed scala aan stoffen kan oplossen.
* Essentieel voor het leven: Water is cruciaal voor alle levende organismen.
Interacties van KCl en water
* Oplossen: Kaliumchloride lost gemakkelijk op in water. Wanneer het is opgelost, dissocieert het in de samenstellende ionen (K⁺ en Cl⁻), die omgeven worden door watermoleculen. Dit proces staat bekend als hydratatie .
* Oplossingen: Oplossingen van kaliumchloride in water worden vaak gebruikt in verschillende toepassingen:
* Landbouwirrigatie: KCl-oplossingen worden gebruikt om planten van kalium te voorzien.
* Medische oplossingen: KCl-oplossingen worden gebruikt in intraveneuze vloeistoffen om de kaliumspiegels in het lichaam aan te vullen.
* Chemische reacties: KCl-oplossingen worden gebruikt als reactanten of reagentia bij chemische reacties.
Belangrijke opmerking:
* Concentraties: De concentratie kaliumchloride in water kan de eigenschappen ervan aanzienlijk beïnvloeden. Hogere concentraties kunnen leiden tot een hogere geleidbaarheid en veranderingen in de pH van de oplossing.
* Veiligheid: Hoewel kaliumchloride in kleine hoeveelheden over het algemeen veilig is, is het belangrijk om je bewust te zijn van de potentiële toxiciteit ervan bij hogere concentraties.
Samenvattend zijn kaliumchloride en water essentiële verbindingen die met elkaar samenwerken om oplossingen te vormen met diverse toepassingen op verschillende gebieden. Het begrijpen van hun eigenschappen en interacties is cruciaal voor een veilig en effectief gebruik ervan.
 Wat zijn de coëfficiënten voor reactie N2H4 plus H2O2 en N2 H2O?
Wat zijn de coëfficiënten voor reactie N2H4 plus H2O2 en N2 H2O?  Tot welk element zuurstof, weergegeven door het symbool O, wordt geclassificeerd?
Tot welk element zuurstof, weergegeven door het symbool O, wordt geclassificeerd?  Welke twee woorden beschrijven magnesiumchloride?
Welke twee woorden beschrijven magnesiumchloride?  Hoe kan een grote hoeveelheid door water oplosbare vaste stoffen worden verwijderd?
Hoe kan een grote hoeveelheid door water oplosbare vaste stoffen worden verwijderd?  Hoe werd bewezen dat de hele massa van een atoom zich in het midden bevindt?
Hoe werd bewezen dat de hele massa van een atoom zich in het midden bevindt?
 Waarom is er meer stof in warme omgevingen dan in koude omgevingen?
Waarom is er meer stof in warme omgevingen dan in koude omgevingen?  Het Parkfield-segment van de San Andreas-fout kan af en toe grote aardbevingen bevatten
Het Parkfield-segment van de San Andreas-fout kan af en toe grote aardbevingen bevatten Hoe te stoppen met vogels van tsjilpen de hele nacht lang
Hoe te stoppen met vogels van tsjilpen de hele nacht lang  Wat is institutionele vrouwenhaat bij de politie? Onderzoek laat zien hoe het eruit ziet – en waarom het ertoe doet
Wat is institutionele vrouwenhaat bij de politie? Onderzoek laat zien hoe het eruit ziet – en waarom het ertoe doet  Is het universum werkelijk een ‘donker bos’ vol vijandige buitenaardse wezens die zich schuilhouden?
Is het universum werkelijk een ‘donker bos’ vol vijandige buitenaardse wezens die zich schuilhouden?
Hoofdlijnen
- Wat is de wetenschappelijke naam voor een shag met blauwe ogen?
- De genetische informatie wordt door DNA gecodeerd door?
- Wat is de gecontroleerde variabele in experiment over spontane generatie?
- Welke van deze structuren is uniek voor plantencellen?
- Waarom heterotrofen zijn afhankelijk van autotrofen.
- Welke organellen missen erytrocyten?
- In de meeste Biotechnology Research Laboratories Welk dier zou je vinden?
- Wat is de conclusie voor cellen?
- Hoe verschilt polygene eigenschap van eenvoudige overerving?
- Kleine aminozuurverschillen kunnen leiden tot dramatisch verschillende enzymen
- Video:Zijn bacteriën de toekomst van olierampen en het opruimen van radioactief afval?

- Zout zet een snelle stap voordat het uit het water valt

- Minder vocht in natuurlijke vezels

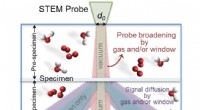
- Bepaling van de parameters voor transmissie-elektronenmicroscopie
 Wanneer een uitgerekte snaar wordt vrijgegeven, is de potentiële energie die wordt omgezet in.
Wanneer een uitgerekte snaar wordt vrijgegeven, is de potentiële energie die wordt omgezet in.  Waarom is neerslag overvloediger aan één kant E van de berg?
Waarom is neerslag overvloediger aan één kant E van de berg?  Scanning tunneling microscopie:computersimulaties verscherpen inzichten in moleculen
Scanning tunneling microscopie:computersimulaties verscherpen inzichten in moleculen Wat gebeurt er met catechol -oxidase wanneer de pH aan weerszijden van het optimum staat?
Wat gebeurt er met catechol -oxidase wanneer de pH aan weerszijden van het optimum staat?  Wat is het exacte aantal organische verbindingen?
Wat is het exacte aantal organische verbindingen?  Kunnen ballonnen op grote hoogte bosbranden helpen voorspellen?
Kunnen ballonnen op grote hoogte bosbranden helpen voorspellen?  Hoe wordt de fase van een ster genaamd waar het gewoon afkoelt en vervaagt?
Hoe wordt de fase van een ster genaamd waar het gewoon afkoelt en vervaagt?  Meiotische celdeling vindt plaats in een speciaal orgaan dat bekend staat als?
Meiotische celdeling vindt plaats in een speciaal orgaan dat bekend staat als?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

