
Wetenschap
Chlooroxidatiegetal:inzicht in -1 en zijn rol
Dit is waarom:
* Chloor is een halogeen: Halogenen bevinden zich in groep 17 van het periodiek systeem en zijn zeer elektronegatief. Dit betekent dat ze de neiging hebben om elektronen te verkrijgen om een stabiel octet te bereiken.
* Een elektron verkrijgen: Wanneer chloor een elektron verkrijgt, bereikt het een lading van -1, dus het oxidatiegetal is -1.
* Voorbeelden: In verbindingen als NaCl (natriumchloride) en HCl (zoutzuur) heeft chloor een oxidatiegetal van -1.
Het is echter belangrijk op te merken dat chloor andere oxidatiegetallen kan vertonen, afhankelijk van de verbinding waarin het zich bevindt. Bijvoorbeeld:
* +1 in HOCl (hypochloorzuur)
* +3 in HClO2 (chloorzuur)
* +5 in HClO3 (chloorzuur)
* +7 in HClO4 (perchloorzuur)
* 0 in Cl2 (chloorgas)
 Hoe is het mogelijk dat een verbinding zowel ionische als covalente bindingen heeft?
Hoe is het mogelijk dat een verbinding zowel ionische als covalente bindingen heeft?  Wat zijn sulfaten?
Wat zijn sulfaten?  Wat is de atomische massa Pottasium?
Wat is de atomische massa Pottasium?  Wat is de roze vaste stof gevormd als Millennium toegevoegd aan kopersulfaatoplossing?
Wat is de roze vaste stof gevormd als Millennium toegevoegd aan kopersulfaatoplossing?  Onderzoekers verbeteren de plasticiteit van keramische materialen bij kamertemperatuur
Onderzoekers verbeteren de plasticiteit van keramische materialen bij kamertemperatuur
 Innovatieve technologieën en beleid kunnen de landbouw ecologisch duurzaam maken
Innovatieve technologieën en beleid kunnen de landbouw ecologisch duurzaam maken Onderzoekers ontdekken de belangrijkste reactie die de groei van potentieel schadelijke deeltjes in de atmosfeer beïnvloedt
Onderzoekers ontdekken de belangrijkste reactie die de groei van potentieel schadelijke deeltjes in de atmosfeer beïnvloedt Plantenpigmenten Gevonden in Spinazie
Plantenpigmenten Gevonden in Spinazie  Boek onderzoekt hoe bomen veranderen naarmate ze ouder worden en groeien:wat vertellen deze aanwijzingen ons?
Boek onderzoekt hoe bomen veranderen naarmate ze ouder worden en groeien:wat vertellen deze aanwijzingen ons?  Natuurbranden hebben invloed op de waterkwaliteit
Natuurbranden hebben invloed op de waterkwaliteit
Hoofdlijnen
- Hoe beïnvloedt het type plant transpiratie?
- Gaan we het nu echt over walvissen hebben?
- Een muis of een olifant:welke soort bestrijdt infecties effectiever?
- Wat is de evolutionaire betekenis van de genetische codes bij Universaliteit?
- Een organisme dat een bron van energie of geschikte omgeving biedt voor virus een ander om te leven?
- Wat is het tweede trofische niveau in Food Web?
- Waarom zijn worteltip- en embryocellen goed voor het bestuderen van mitose?
- Wat is de meeste uitleg voor hoe speciaties optreden?
- Wat zijn structuur het bevattende DNA genoemd?
- In vivo geneesmiddelontdekking voor het verhogen van incretine tot expressie brengende cellen bij diabetes

- Bruggen bouwen tussen atomen en hoogwaardige katalysatoren maken

- Een sessiele druppel optillen van een superamfifoob oppervlak met behulp van een inslaande druppel
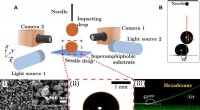
- Eenvoudige watertest kan verlammende botziekte voorkomen

- Elektronen versterken de calorische koeling in vaste toestand in hexagonale sulfiden

 Wat is de corona rond de maan?
Wat is de corona rond de maan?  Waarom komt de zon twee uur eerder op in het oosten dan het westen?
Waarom komt de zon twee uur eerder op in het oosten dan het westen?  Hoe kunnen de vier niveaus van organisatie in levende wezens meercellige organismen in staat stellen werklevenprocessen te verdelen?
Hoe kunnen de vier niveaus van organisatie in levende wezens meercellige organismen in staat stellen werklevenprocessen te verdelen?  Onderzoek onthult verschillen in DNA-vouwing tussen neuronen en andere hersencellen en koppelt deze aan celfuncties
Onderzoek onthult verschillen in DNA-vouwing tussen neuronen en andere hersencellen en koppelt deze aan celfuncties  Welk type materiaal is een isolator?
Welk type materiaal is een isolator?  Tropische cyclonen:hoe ze bijdragen aan betere voorspellingen op het maritieme continent
Tropische cyclonen:hoe ze bijdragen aan betere voorspellingen op het maritieme continent Wat zou lysosoom zijn is een cel was school?
Wat zou lysosoom zijn is een cel was school?  Hoe mantelbewegingen het aardoppervlak bepalen
Hoe mantelbewegingen het aardoppervlak bepalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

