
Wetenschap
Inzicht in de toestanden van materie voor covalente verbindingen
Solid State:
* Sterke covalente bindingen: De covalente bindingen binnen het molecuul zijn sterk en houden de atomen stevig bij elkaar.
* Intermoleculaire krachten: Hoewel de bindingen binnen het molecuul sterk zijn, kunnen de krachten tussen moleculen (zoals van der Waals-krachten of waterstofbruggen) in sterkte variëren.
* Arrangement: In vaste stoffen houden deze intermoleculaire krachten de moleculen in een vaste, regelmatige opstelling, waardoor een stijve structuur ontstaat.
Vloeibare toestand:
* Zwakkere intermoleculaire krachten: In vloeistoffen zijn de intermoleculaire krachten zwakker vergeleken met de vaste toestand, waardoor moleculen vrijer kunnen bewegen.
* Vloeiende aard: De moleculen kunnen langs elkaar heen glijden, waardoor vloeistoffen hun karakteristieke vloeibare karakter krijgen.
Gasvormige toestand:
* Zeer zwakke intermoleculaire krachten: In gassen zijn de intermoleculaire krachten extreem zwak. Hierdoor kunnen moleculen willekeurig en onafhankelijk bewegen en de hele container waarin ze zich bevinden vullen.
* Hoge kinetische energie: Gasmoleculen bezitten een hoge kinetische energie, waardoor ze snel kunnen bewegen en regelmatig kunnen botsen.
Factoren die de toestand van de materie beïnvloeden:
* Moleculaire grootte: Grotere moleculen hebben over het algemeen sterkere intermoleculaire krachten, waardoor het waarschijnlijker is dat ze bij kamertemperatuur vloeistoffen of vaste stoffen zijn.
* Polariteit: Polaire moleculen hebben sterkere intermoleculaire krachten (dipool-dipoolinteracties) dan niet-polaire moleculen, waardoor het waarschijnlijker is dat ze vloeistoffen of vaste stoffen zijn.
* Waterstofbinding: Verbindingen die in staat zijn tot waterstofbinding (zoals water) hebben zeer sterke intermoleculaire krachten, die hun fysieke toestand beïnvloeden.
* Temperatuur: Het verhogen van de temperatuur levert meer kinetische energie aan moleculen, waardoor de intermoleculaire krachten worden verzwakt en de vloeibare of gasvormige toestand wordt bevorderd.
* Druk: Toenemende druk dwingt moleculen dichter bij elkaar, waardoor de intermoleculaire krachten toenemen en de vloeibare of vaste toestand wordt begunstigd.
Voorbeelden:
* Vast: Diamant (covalente vaste stof uit het netwerk), suiker (covalente vaste stof met sterke intermoleculaire krachten)
* Vloeistof: Water (covalente vloeistof met sterke waterstofbinding), alcohol (covalente vloeistof met matige intermoleculaire krachten)
* Gas: Zuurstof (covalent gas met zwakke intermoleculaire krachten), kooldioxide (covalent gas met zwakke intermoleculaire krachten)
Samenvattend hangt de toestand van een covalente verbinding af van de balans tussen de sterkte van de covalente bindingen binnen het molecuul en de sterkte van de intermoleculaire krachten tussen moleculen.
 Hoe u kunt bepalen of een stof zuur is:een praktische gids
Hoe u kunt bepalen of een stof zuur is:een praktische gids  Welk volume fosforzuur met een molariteit van 0,200 zal volledig reageren met 50 ml natriumhydroxide van 0,100?
Welk volume fosforzuur met een molariteit van 0,200 zal volledig reageren met 50 ml natriumhydroxide van 0,100?  Nieuwe katalysator zet kooldioxide uit industriële emissies om in veelgebruikte chemicaliën
Nieuwe katalysator zet kooldioxide uit industriële emissies om in veelgebruikte chemicaliën  Het proces van scheiding F mengsel kamfer en natriumchloride?
Het proces van scheiding F mengsel kamfer en natriumchloride?  Hoe verschillen vaste stoffen, vloeistoffen en gassen, deeltjes?
Hoe verschillen vaste stoffen, vloeistoffen en gassen, deeltjes?
 Vergelijk en contrasteer de natuurlijke selectie -evolutie?
Vergelijk en contrasteer de natuurlijke selectie -evolutie?  Green Deal:Goed voor een klimaatneutraal Europa, slecht voor de planeet
Green Deal:Goed voor een klimaatneutraal Europa, slecht voor de planeet Sentinel-2-satellieten die worden gebruikt voor de doorlopende monitoring van graslanden
Sentinel-2-satellieten die worden gebruikt voor de doorlopende monitoring van graslanden Een nieuwe studie toont aan dat Amerikanen dieper dan ooit boren naar zoet water
Een nieuwe studie toont aan dat Amerikanen dieper dan ooit boren naar zoet water Wat is de naam van hoeveelheid licht die een object reflecteert ten opzichte van zijn omgeving?
Wat is de naam van hoeveelheid licht die een object reflecteert ten opzichte van zijn omgeving?
Hoofdlijnen
- Wat is de grootste boom geboren fruit?
- Hoe adhesief eiwit malaria veroorzaakt
- Doel van pepsine in DNA -extract?
- Wat gebeurt er wanneer een organisme zich in tweeën verdeelt om nakomelingen te produceren?
- Welke organel produceert enzymen?
- Aminozuren zijn de bouwstenen van eiwitten.
- Wat beschrijft het beste de structuur van een DNA-molecuul-?
- Wat is atenologie?
- Hoe leren wetenschappers over uitgestorven soorten?
- Door bacteriën gekweekte gebouwen:nieuw onderzoek om cellen in minifabriekjes voor materialen te veranderen

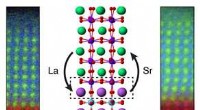
- Het benutten van verloren atomen kan helpen bij het maken van nieuwe, nooit eerder vertoonde oxiden
- Polymeren met verschillende lengtes kweken

- Nylon neemt eindelijk zijn plaats in als piëzo-elektrisch textiel

- Bepalen of een oplossing neutraal, basisch of zuur is (pH-identificatietechnieken)

 Is zwavelzuur zuurder dan citroensap?
Is zwavelzuur zuurder dan citroensap?  Sterke groei van het aantal abonnees verhoogt de omzet van Netflix, winst (update)
Sterke groei van het aantal abonnees verhoogt de omzet van Netflix, winst (update) Kankeronderzoek kan bijwerkingen van chemotherapie verminderen
Kankeronderzoek kan bijwerkingen van chemotherapie verminderen Hoe een handvol prehistorische genieën de technologische revolutie van de mensheid lanceerden
Hoe een handvol prehistorische genieën de technologische revolutie van de mensheid lanceerden  Qubits samengesteld uit gaten kunnen de truc zijn om sneller te bouwen, grotere kwantumcomputers
Qubits samengesteld uit gaten kunnen de truc zijn om sneller te bouwen, grotere kwantumcomputers Vierkante voet naar Yards
Vierkante voet naar Yards Waarom heeft berylliumchloride een meer covalent karakter dan bariumchloride?
Waarom heeft berylliumchloride een meer covalent karakter dan bariumchloride?  Welk weefsel vormt de opperhuid?
Welk weefsel vormt de opperhuid?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

