
Wetenschap
Redoxreacties uitgelegd:elektronenoverdracht en chemische processen
Redoxreacties:een dans van elektronenoverdracht
De kern van een redoxreactie ligt in de overdracht van elektronen tussen reactanten. Hier is hoe het werkt:
* Oxidatie: Eén reactant verliest elektronen. We zeggen dat het *geoxideerd* is. Zie het als het verliezen van een negatieve lading, waardoor de reactant positiever wordt.
* Reductie: Een andere reactant wint de elektronen die verloren zijn gegaan door de eerste reactant. We zeggen dat het *verlaagd* is. Zie het als het verkrijgen van een negatieve lading, zodat de reactant negatiever wordt.
Belangrijkste punten
* Altijd samen: Bij een redoxreactie vinden oxidatie en reductie altijd gelijktijdig plaats. Je kunt het één niet hebben zonder het ander.
* LEO zegt GER: Een handig geheugensteuntje om te onthouden:L ose E elektronen O xidatie, G ain E elektronen R onderwijs.
Voorbeeld:roesten van ijzer
* IJzer (Fe) wordt geoxideerd: Het verliest elektronen om ijzerionen (Fe²⁺) te vormen.
* Zuurstof (O₂) wordt verminderd: Het wint de elektronen terug die verloren gaan door ijzer, waardoor oxide-ionen (O²⁻) worden gevormd.
Belangrijkste concepten
* Oxidatiemiddel: De reactant die ervoor zorgt dat een andere reactant wordt geoxideerd. In het roestvoorbeeld is zuurstof het oxidatiemiddel.
* Reduceermiddel: De reactant die ervoor zorgt dat een andere reactant wordt gereduceerd. IJzer is het reductiemiddel in het roestvoorbeeld.
* Redoxreacties in het dagelijks leven: Redoxreacties zijn essentieel voor veel processen:
* Ademhaling: Ons lichaam gebruikt glucose als brandstof en oxideert het om energie vrij te maken.
* Fotosynthese: Planten gebruiken zonlicht om kooldioxide en water om te zetten in glucose, een proces waarbij redoxreacties betrokken zijn.
* Batterijen: De stroom van elektronen in batterijen is een klassiek voorbeeld van een redoxreactie.
Laat het me weten als je meer voorbeelden wilt zien of specifieke soorten redoxreacties wilt verkennen. Ik ben hier om te helpen!
 Eilandbewoners in de Stille Oceaan hebben Antarctica waarschijnlijk als eerste gevonden:studie
Eilandbewoners in de Stille Oceaan hebben Antarctica waarschijnlijk als eerste gevonden:studie Wat zijn het ecosysteemhuis van de apen?
Wat zijn het ecosysteemhuis van de apen?  De kliffen van Zuid-Californië verliezen het einde van de stijgende zee
De kliffen van Zuid-Californië verliezen het einde van de stijgende zee Welk effect heeft zure regen op vegetatie waar het valt?
Welk effect heeft zure regen op vegetatie waar het valt?  Modet de groene toekomst van zeewierjassen en paddenstoelenschoenen
Modet de groene toekomst van zeewierjassen en paddenstoelenschoenen
Hoofdlijnen
- Wat is de naam voor een reactie die monomeren verbindt om een voedselketen te vormen?
- Hoe wordt de kloof tussen tanden van een herbivoor genoemd?
- Wat is de functie van microbiologie?
- Is het een neushoorn? Nieuwe DNA-test identificeert hoorns sneller om stropers te vangen
- Welke lichaamscellen ondergaan mesiose?
- Wormen verhogen het fosfaatgehalte in gras
- Smartphone-app gebruikt computervisie om verloren dieren te identificeren
- Een orchidee die nooit bloeit
- Welk type reproductie resulteert in de genetische variatie van de grootste hoeveelheid?
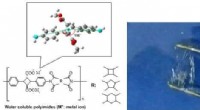
- Hoog-thermoresistente biopolyimiden worden in water oplosbaar zoals zetmeel
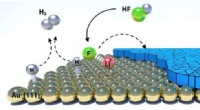
- Batterijen verborgen laag onthuld
- Nieuwe stikstof-assemblage koolstofkatalysator heeft potentieel om chemische productie te transformeren

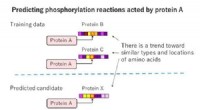
- Fujitsu ontwikkelt technologie om biochemische reacties te voorspellen, opheldering van de mechanismen van genetische aandoeningen
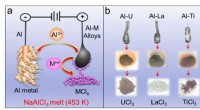
- Wetenschappers stellen IAP-proces voor voor scheiding van aluminiumlegeringen
 Wat is het beste voorbeeld van een stuk machines of apparatuur die radiologische energiebron bevat?
Wat is het beste voorbeeld van een stuk machines of apparatuur die radiologische energiebron bevat?  Wat is de natuurlijke habitat voor meelwormen?
Wat is de natuurlijke habitat voor meelwormen?  Wanneer dode planten en dieren uiteenvallen, wat gebeurt er dan met de kwestie waar het van heeft gemaakt?
Wanneer dode planten en dieren uiteenvallen, wat gebeurt er dan met de kwestie waar het van heeft gemaakt?  Foxconn-leiders, functionarissen van Wisconsin ontmoeten elkaar; details onduidelijk
Foxconn-leiders, functionarissen van Wisconsin ontmoeten elkaar; details onduidelijk Een delicaat evenwicht:nieuw onderzoek laat zien hoe netwerken zichzelf gesynchroniseerd houden
Een delicaat evenwicht:nieuw onderzoek laat zien hoe netwerken zichzelf gesynchroniseerd houden  Wat is de snelheid als u in een cirkel van 10 mijl reist op 14 km / u en eindigt waar begonnen?
Wat is de snelheid als u in een cirkel van 10 mijl reist op 14 km / u en eindigt waar begonnen?  BMW in het gareel voor geld terwijl Duitse autoverkopen kelderen
BMW in het gareel voor geld terwijl Duitse autoverkopen kelderen Japan, de thuisbasis van de hightech wc, hoopt dat een basistoilet levens kan redden
Japan, de thuisbasis van de hightech wc, hoopt dat een basistoilet levens kan redden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

