
Wetenschap
Inzicht in de chemische opbrengst:theoretische versus werkelijke opbrengsten
Dit is waarom:
* Theoretisch rendement: Dit is de maximale hoeveelheid product die kan worden gevormd als de reactie voltooid is en alle reactanten in producten zijn omgezet. Het wordt berekend op basis van stoichiometrie.
* Werkelijke opbrengst: Dit is de hoeveelheid product die daadwerkelijk in het laboratorium wordt verkregen. Het is altijd minder dan de theoretische opbrengst.
Redenen voor minder dan theoretisch rendement:
* Onvolledige reacties: Het is mogelijk dat niet alle reactanten reageren om producten te vormen.
* Nevenreacties: Andere reacties kunnen tegelijkertijd plaatsvinden, waarbij een deel van de reactanten wordt verbruikt.
* Verlies tijdens isolatie: Tijdens het zuiverings- en isolatieproces kan een deel van het product verloren gaan.
* Evenwicht: Sommige reacties bereiken een evenwichtspunt waar de voorwaartse en achterwaartse reacties met dezelfde snelheid plaatsvinden, waardoor de hoeveelheid gevormd product wordt beperkt.
* Onzuiverheden: De uitgangsmaterialen of het reactiemengsel kunnen onzuiverheden bevatten die de reactie beïnvloeden.
Opbrengstpercentage:
Om de efficiëntie van een reactie te kwantificeren, gebruiken we het opbrengstpercentage :
Percentage opbrengst =(werkelijke opbrengst / theoretische opbrengst) * 100%
 Wat is de uitvinding die vloeistoffen gebruikt, zijn erg koud en absorberen warmte?
Wat is de uitvinding die vloeistoffen gebruikt, zijn erg koud en absorberen warmte?  Wat is moleculaire opstelling?
Wat is moleculaire opstelling?  Hoe kan een tabellijst van metalen in een activiteitenreeks nuttig zijn om voor te gaan of chemische reactie zal optreden?
Hoe kan een tabellijst van metalen in een activiteitenreeks nuttig zijn om voor te gaan of chemische reactie zal optreden?  AI-agent helpt materiaaleigenschappen sneller te identificeren
AI-agent helpt materiaaleigenschappen sneller te identificeren Is het oplossen van zout in water een chemische verandering?
Is het oplossen van zout in water een chemische verandering?
 Seal brengt gegevens over het warmtetransport van de oceaan naar nieuwe diepten
Seal brengt gegevens over het warmtetransport van de oceaan naar nieuwe diepten Waarom zijn ondiepe meren gevoelig voor eutrofiëring?
Waarom zijn ondiepe meren gevoelig voor eutrofiëring?  Een Europa bedekt met graslanden of bossen:innovatie en onderzoek naar klimaatmodellen
Een Europa bedekt met graslanden of bossen:innovatie en onderzoek naar klimaatmodellen Holoceentemperatuur op het Iberisch schiereiland gereconstrueerd met subfossielen van insecten
Holoceentemperatuur op het Iberisch schiereiland gereconstrueerd met subfossielen van insecten Kunnen startups het instrument zijn om klimaatverandering op te lossen?
Kunnen startups het instrument zijn om klimaatverandering op te lossen?
Hoofdlijnen
- Een plaag van onze eigen makelij:het onthullen van de ware oorsprong van de niet zo Duitse kakkerlak
- Welke subklasse van lipiden is belangrijk in de membraanstructuur?
- Waarom kneden katten?
- Zijn alle organismen hetzelfde in de eerste fase van ontwikkeling?
- Welk type weefsel bevat cellen die neuronen worden genoemd?
- Wat is het eerste orgel dat zich in embryo ontwikkelt?
- Voorbij kroontjeskruid:het creëren van een migratieoase voor monarchen
- Wat doen wetenschappers wanneer een nieuw ontdekt organisme niet in een exsisterende categorie past?
- Drie verschillen tussen biotische en abiotische componenten van een ecosysteem?
- Kleine medicijnafgiftecapsules kunnen getransplanteerde insulineproducerende cellen ondersteunen
- Naar kosteneffectieve oplossingen voor de volgende generatie consumentenelektronica, elektrische voertuigen en elektriciteitsnetten
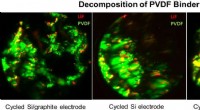
- Kunstmatige intelligentie helpt bij de fabricage van materialen

- Onderzoekers ontwikkelen nieuwe strategie voor efficiënte OLED-schermen met actieve matrix

- Een nieuwe manier om pompoenkruiden te maken, verdovende middelen, cosmetica

 Optische gegevensverwerking profiteert van nieuw soort mobiliteit
Optische gegevensverwerking profiteert van nieuw soort mobiliteit De vloeistofstroom door een gat in een buis berekenen
De vloeistofstroom door een gat in een buis berekenen Twee miljard jaar oude zoutrots onthult stijging van zuurstof in oude atmosfeer
Twee miljard jaar oude zoutrots onthult stijging van zuurstof in oude atmosfeer Hoe een fractie in tweeën te verdelen
Hoe een fractie in tweeën te verdelen Welk element heeft dezelfde valentie-elektronenconfiguratie als fosfor?
Welk element heeft dezelfde valentie-elektronenconfiguratie als fosfor?  Waarom Comets Halley is een slecht voorteken?
Waarom Comets Halley is een slecht voorteken?  Wat was het instrument dat celverkenning maakte mogelijke microscoop?
Wat was het instrument dat celverkenning maakte mogelijke microscoop?  Hoeveel mol atomen zitten er in 1,00 lb lood?
Hoeveel mol atomen zitten er in 1,00 lb lood?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

