
Wetenschap
Vitamine B12:bio-anorganische chemie, structuur en belangrijkste reacties
Bio-anorganische en supramoleculaire chemie van vitamine B12:belangrijke reacties
Vitamine B12, ook bekend als cobalamine, is een complexe organometaalcofactor die essentieel is voor verschillende enzymatische reacties in het menselijk lichaam. De structuur en reactiviteit ervan zijn fascinerende onderwerpen binnen de bio-anorganische en supramoleculaire chemie.
Structuur van vitamine B12:
* Corrin-ring: De kern van vitamine B12 is een macrocyclisch ringsysteem genaamd corrin, dat lijkt op porfyrine maar met één methinebrug minder.
* Kobaltion (Co(III)): Het centrale metaalion is kobalt in zijn +3 oxidatietoestand, gecoördineerd met vier stikstofatomen van de corrin-ring, één axiale stikstof uit de 5,6-dimethylbenzimidazool (DMB) base en een variabel zesde ligand.
* Axiale liganden: Het zesde ligand is cruciaal voor de reactiviteit van vitamine B12. Het kan een verscheidenheid aan moleculen zijn, waaronder water, cyanide, hydroxyl of het substraat in een enzymatische reactie.
Belangrijkste reacties van vitamine B12:
Vitamine B12 is betrokken bij twee primaire enzymatische reacties:
1. Methyleringsreacties: Vitamine B12 is een cofactor voor methyltransferasen , zoals tetrahydrofolaatreductase (THF-reductase) en methioninesynthase . Bij deze reacties ondergaat het kobaltion een redoxcyclus van één elektron tussen Co(I) en Co(III).
* Co(I) staat: Zeer nucleofiel, in staat methylgroepen te binden.
* Co(III)-status: Stabieler, kan de methylgroep naar het substraat overbrengen.
2. Herschikkingsreacties: Vitamine B12 is een cofactor voor isomerasen , zoals methylmalonyl-CoA-mutase . Deze enzymen katalyseren de intramoleculaire herschikking van functionele groepen binnen een molecuul.
* Adenosylcobalamine (AdoB12): Deze vorm van vitamine B12, waarbij het zesde ligand een 5'-deoxyadenosylgroep is, is cruciaal voor herschikkingen.
* Co(I) staat: De Co-C-binding in AdoB12 is zwak en kan homolytisch splitsen, waardoor een zeer reactief kobalt(II)radicaal ontstaat. .
* Radicaal mechanisme: Het kobaltradicaal onttrekt een waterstofatoom aan het substraat en initieert een reeks radicaalreacties die tot de gewenste isomerisatie leiden.
Supramoleculaire aspecten van vitamine B12:
* Enzym-cofactor-interacties: De specifieke binding van vitamine B12 aan enzymen is cruciaal voor de activiteit ervan. Het enzym zorgt voor de specifieke omgeving voor de reactie en stabiliseert de reactieve tussenproducten.
* Niet-covalente interacties: Waterstofbruggen, elektrostatische interacties en hydrofobe effecten spelen een belangrijke rol bij de herkenning en binding van vitamine B12 aan zijn enzympartners.
* Eiwitgemedieerde levering: Vitamine B12 wordt door specifieke eiwitten in het lichaam getransporteerd, waardoor een efficiënte levering aan doelcellen en organen wordt gegarandeerd.
Betekenis van bio-anorganische en supramoleculaire chemie in vitamine B12-onderzoek:
* Mechanismen begrijpen: Deze velden bieden cruciale inzichten in de reactiemechanismen van vitamine B12-afhankelijke enzymen.
* Nieuwe therapieën ontwerpen: Het begrijpen van de structuur en reactiviteit van vitamine B12 helpt bij de ontwikkeling van nieuwe medicijnen en therapieën voor vitamine B12-tekortstoornissen.
* Nieuwe katalysatoren ontwikkelen: De unieke reactiviteit van vitamine B12 inspireert het ontwerp van nieuwe katalysatoren voor organische synthese.
Conclusie:
Het ingewikkelde samenspel van bio-anorganische en supramoleculaire chemie binnen de structuur en reactiviteit van vitamine B12 benadrukt het belang ervan in het leven. Het begrijpen van de ingewikkelde details van zijn interacties met enzymen en zijn vermogen om deel te nemen aan complexe reacties is cruciaal voor het ontwikkelen van nieuwe strategieën voor het verbeteren van de menselijke gezondheid en het verkennen van nieuwe grenzen op het gebied van katalyse.
 Wat is het verschil tussen NADH en NADPH?
Wat is het verschil tussen NADH en NADPH?  Hebben alle stoffen hun eigen kookpunt en vriespunt?
Hebben alle stoffen hun eigen kookpunt en vriespunt?  Welke verbinding kan ontleding ondergaan om bariumchloride en zuurstof te produceren?
Welke verbinding kan ontleding ondergaan om bariumchloride en zuurstof te produceren?  Welk volume van 0,150 M HCLO4-oplossing is nodig om 60 ml 0F 8.6510-2M NaOH te neutraliseren?
Welk volume van 0,150 M HCLO4-oplossing is nodig om 60 ml 0F 8.6510-2M NaOH te neutraliseren?  Karamelkleur is het organisch of anorganisch?
Karamelkleur is het organisch of anorganisch?
 De cyclus van zuurstof door een ecosysteem
De cyclus van zuurstof door een ecosysteem  Wat vonden mensen van de structuur van de aarde?
Wat vonden mensen van de structuur van de aarde?  Hoe snel kunnen we voorkomen dat de aarde opwarmt?
Hoe snel kunnen we voorkomen dat de aarde opwarmt? Gemeenschappelijke spinnen in Zuid-Afrika
Gemeenschappelijke spinnen in Zuid-Afrika Uit onderzoek blijkt dat de emissies van stortplaatsbronnen een buitensporige impact hebben en kansen bieden om Amerikaans afvalmethaan aan te pakken
Uit onderzoek blijkt dat de emissies van stortplaatsbronnen een buitensporige impact hebben en kansen bieden om Amerikaans afvalmethaan aan te pakken
Hoofdlijnen
- Hoge opbrengst, eiwit met sojabonengen
- Wat is een mutatie en waarom zijn mutaties belangrijk in evolutie?
- Lijkt ATP meer op RNA of DNA?
- Hoe is vertaling in de biologie vergelijkbaar met taalvertaling?
- Ooglidtrekkingen begrijpen:oorzaken, wanneer het er toe doet, en deskundige oplossingen
- Welke wetenschappelijke naam voor flagella?
- Wat is het wetenschappelijke woord voor kont?
- Bestaat de opperhuid uit levende en dode huidcellen?
- Is het mogelijk voor een andere diersoort om te evolueren als mensen?
- Wanneer minder meer is:Designer-spleten maken glasachtige materialen veel sterker

- Gevoelstemperatuur beheersen:hoe u de waargenomen temperatuur nauwkeurig kunt berekenen

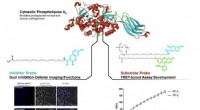
- Fluorescerende sondes om cellulaire activiteit te bestuderen
- Een nieuwe bindingsplaats voor antibiotica gevonden in het ribosoom
- Bierafval scheiden in eiwitten voor voedingsmiddelen, en vezels voor biobrandstoffen

 Springende hagedissen:onderzoek test de grenzen van gekko-adhesie
Springende hagedissen:onderzoek test de grenzen van gekko-adhesie Welke winning van zout uit zeewater?
Welke winning van zout uit zeewater?  18 gauge is gelijk aan hoeveel mm?
18 gauge is gelijk aan hoeveel mm?  Hoe HeLa-cellen werken
Hoe HeLa-cellen werken  Wat heeft meer energie iets heet of koud?
Wat heeft meer energie iets heet of koud?  Aanvaarding van elektrische voertuigen verbetert de luchtkwaliteit en klimaatvooruitzichten
Aanvaarding van elektrische voertuigen verbetert de luchtkwaliteit en klimaatvooruitzichten Welke laboratoriumapparatuur wordt gebruikt om de tijd te meten?
Welke laboratoriumapparatuur wordt gebruikt om de tijd te meten?  Wat dronken ze? Onderzoekers onderzoeken radioactieve crockpots
Wat dronken ze? Onderzoekers onderzoeken radioactieve crockpots
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

