
Wetenschap
Katalysatoren:hun rol in chemische reacties begrijpen
Katalysatoren de snelheid van een chemische reactie versnellen zonder daarbij verbruikt te worden. Ze bieden een alternatieve route voor de reactie met een lagere activeringsenergie, waardoor het voor de reactanten gemakkelijker wordt om producten te vormen.
Voorbeelden van katalysatoren:
* Enzymen: Biologische katalysatoren die biochemische reacties in levende organismen versnellen.
* Metaalkatalysatoren: Gebruikt in veel industriële processen, zoals de productie van benzine en kunststoffen.
* Zuurkatalysatoren: Gebruikt in veel organische reacties, zoals verestering en dehydratatie.
Belangrijkste kenmerken van katalysatoren:
* Ze worden niet verbruikt bij de reactie.
* Ze verlagen de activeringsenergie van de reactie.
* Ze versnellen de reactiesnelheid.
* Ze hebben geen invloed op de evenwichtspositie van de reactie.
 Vee grazen met virtuele omheining toont potentieel om brandstofonderbrekingen voor natuurbranden te creëren, studie vondsten
Vee grazen met virtuele omheining toont potentieel om brandstofonderbrekingen voor natuurbranden te creëren, studie vondsten Japan weegt nog steeds stortplaats radioactief water van Fukushima in oceaan
Japan weegt nog steeds stortplaats radioactief water van Fukushima in oceaan Impact van de mens in een ecosysteem?
Impact van de mens in een ecosysteem?  Vroegste tekenen van leven:wetenschappers vinden microbiële overblijfselen in oude rotsen
Vroegste tekenen van leven:wetenschappers vinden microbiële overblijfselen in oude rotsen Vanuatu geeft wegwerpluiers de spoeling
Vanuatu geeft wegwerpluiers de spoeling
Hoofdlijnen
- Zijn megakaryocyten een soort cel?
- Hoe worden DNA -strengen genoemd?
- 12 gigantische prehistorische dieren en waarom ze krompen
- Wat is bacteriën-rijk?
- Wetenschappers vinden ontbrekende aanwijzing voor de manier waarop HIV-hackcellen zichzelf voortplanten
- Hoe helpen centriolen de cel?
- Zijn de namen die Carolus Linnaeus vandaag nog steeds organismen gaf?
- Welk orgaan doet fotosynthese?
- Wat is de waarschijnlijke bron voor organismen die het beste groeide met 37 graden?
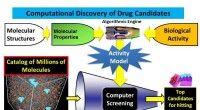
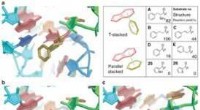
- Algoritme leidt tot een dramatische verbetering van methoden voor het ontdekken van geneesmiddelen
- Legerproject kan leiden tot nieuwe klasse hoogwaardige materialen
- Nieuw promiscue enzym helpt plantenafval om te zetten in duurzame producten

- Moleculaire trillingen benutten om geleidende polymeren te synthetiseren

- Hoe een citroenklok werkt:de wetenschap achter elektrolyse

 Wanneer is Mercurius gevormd?
Wanneer is Mercurius gevormd?  Het definiëren van verwijtbaarheid om AI moreel te maken
Het definiëren van verwijtbaarheid om AI moreel te maken Bevat zeewater twee of meer soorten atomenmoleculen?
Bevat zeewater twee of meer soorten atomenmoleculen?  Team introduceert nieuwe methode om elastische diamanten te laten groeien
Team introduceert nieuwe methode om elastische diamanten te laten groeien Waar in Canada is aardgas gevonden?
Waar in Canada is aardgas gevonden?  Wasberen lossen een eeuwenoude puzzel op, maar begrijpen ze die echt?
Wasberen lossen een eeuwenoude puzzel op, maar begrijpen ze die echt?  Mushroom Hunting in North Idaho
Mushroom Hunting in North Idaho  Burger zoekt nieuwe planeet in zonnestelsel
Burger zoekt nieuwe planeet in zonnestelsel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

