
Wetenschap
Zwak zuur + sterke basereactie:een gedetailleerde uitleg
1. Dissociatie:
* Sterke basis: Een sterke base zoals NaOH dissocieert volledig in water, waardoor hydroxide-ionen (OH-) in de oplossing vrijkomen.
* Zwak zuur: Een zwak zuur zoals azijnzuur (CH3COOH) dissocieert slechts gedeeltelijk in water, waarbij een kleine hoeveelheid waterstofionen (H+) en de geconjugeerde base (CH3COO-) vrijkomen.
2. Neutralisatie:
* De hydroxide-ionen (OH-) van de sterke base reageren met de waterstofionen (H+) van het zwakke zuur om water (H2O) te vormen.
* Deze reactie verbruikt de H+-ionen, waardoor het evenwicht van de dissociatie van het zwakke zuur naar rechts verschuift, waardoor meer van het zwakke zuur dissocieert.
3. Zoutvorming:
* De resterende geconjugeerde base van het zwakke zuur (CH3COO-) combineert met het metaalkation van de sterke base (Na+) om een zout te vormen (natriumacetaat, CH3COONa).
4. pH-verandering:
* De reactie verschuift de pH van de oplossing naar neutraliteit. Omdat de sterke base in overmaat aanwezig is, zal de resulterende oplossing enigszins basisch zijn (pH hoger dan 7).
Belangrijkste kenmerken:
* Buffervorming: Als het zwakke zuur en de geconjugeerde base ervan in aanzienlijke hoeveelheden aanwezig zijn, kan de resulterende oplossing als buffer fungeren en weerstand bieden aan veranderingen in de pH.
* Onvolledige neutralisatie: In tegenstelling tot de reactie van een sterk zuur en een sterke base is de neutralisatie van een zwak zuur door een sterke base niet volledig. Een deel van het zwakke zuur blijft ongedissocieerd, wat leidt tot een enigszins basische oplossing.
Voorbeeld:
Beschouw de reactie van azijnzuur (CH3COOH) met natriumhydroxide (NaOH):
CH3COOH(aq) + NaOH(aq) -> CH3COONa(aq) + H2O(l)
Deze reactie produceert natriumacetaat (CH3COONa), een zout, en water. De oplossing zal een pH hebben die iets hoger is dan 7 vanwege de aanwezigheid van de geconjugeerde base van het zwakke zuur.
Samengevat:
De reactie van een zwak zuur en een sterke base resulteert in neutralisatie, zoutvorming en een enigszins basische oplossing. De resulterende oplossing kan ook als buffer fungeren, afhankelijk van de relatieve concentraties van het zwakke zuur en zijn geconjugeerde base.
 Onderzoek toont aan dat stomerijvloeistof veelbelovend is voor duurzame organische synthese
Onderzoek toont aan dat stomerijvloeistof veelbelovend is voor duurzame organische synthese  Nieuw ontdekt quasikristal werd gecreëerd door de eerste nucleaire explosie op Trinity Site
Nieuw ontdekt quasikristal werd gecreëerd door de eerste nucleaire explosie op Trinity Site Hoe de helderblauwe Med aangespoeld en dood is
Hoe de helderblauwe Med aangespoeld en dood is  Kooldioxide verwijderen uit uitlaatgassen van elektriciteitscentrales
Kooldioxide verwijderen uit uitlaatgassen van elektriciteitscentrales Hoeveel niet -gepaarde elektronen zijn er in de buitenste elektronenschil van chloor?
Hoeveel niet -gepaarde elektronen zijn er in de buitenste elektronenschil van chloor?
 Uit gegevens blijkt dat het begraven van organische koolstof met behulp van klei een vroege Paleozoïsche atmosferische oxygenatie veroorzaakte
Uit gegevens blijkt dat het begraven van organische koolstof met behulp van klei een vroege Paleozoïsche atmosferische oxygenatie veroorzaakte  Biogeochemische verbindingen in Groenland essentieel voor inzicht in het noordpoolgebied
Biogeochemische verbindingen in Groenland essentieel voor inzicht in het noordpoolgebied Maken levende wezens en niet -levende een ecosysteem op?
Maken levende wezens en niet -levende een ecosysteem op?  Welk type milieuwetenschappelijk carrière omvat het verzamelen van informatie over hoe menselijke gebeurtenissen het milieu beïnvloeden?
Welk type milieuwetenschappelijk carrière omvat het verzamelen van informatie over hoe menselijke gebeurtenissen het milieu beïnvloeden?  Wat is het tweede grootste ecosysteem?
Wat is het tweede grootste ecosysteem?
Hoofdlijnen
- Wordt de nakomelingen geproduceerd door conjugatie genetisch identiek aan hun ouders?
- Wat is het primaire molecuul van celmembraan?
- Wat zijn organismen die alle levensprocessen uitvoeren met een enkele cel die wordt genoemd?
- Kunnen taalmodellen het genoom lezen? Deze decodeerde mRNA om betere vaccins te maken
- Het immuunsysteem:bescherming en vitale functies
- Waarom gedijen een gewasplant zoals aardappelen wanneer hun enige waterbron regenwater is?
- Hoe zijn microben nuttig in brood?
- Wat gebeurt er als een cel eiwitten moet maken?
- Wat biedt structuur voor weefsels en organen helpen celmetabolisme uit te voeren?
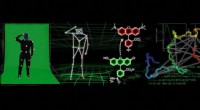
- Chemici ontwikkelen motion capture-achtige technologie voor het volgen van eiwitvorm
- Onthulling wat de kristalgroei regelt

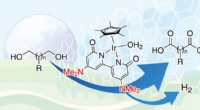
- Team synthetiseert gelijktijdig dicarbonzuren en waterstof uit diolen
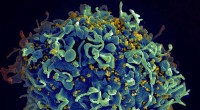
- Wanneer hiv-medicijnen niet meewerken
- De kernelementen van organische moleculen:koolstof, waterstof en zuurstof

 Hoe concurrentie tussen soorten leidde tot een ‘bizar’ patroon in onze eigen evolutionaire stamboom
Hoe concurrentie tussen soorten leidde tot een ‘bizar’ patroon in onze eigen evolutionaire stamboom  Wat is het belang van transport in planten en dieren?
Wat is het belang van transport in planten en dieren?  800 jaar oude middeleeuwse aardewerkfragmenten onthullen Joodse eetgewoonten
800 jaar oude middeleeuwse aardewerkfragmenten onthullen Joodse eetgewoonten Wat draagt genen?
Wat draagt genen?  Hoe déjà vu werkt
Hoe déjà vu werkt  Kashas-regel doorbreken:wetenschappers vinden unieke luminescentie in tetrapod-nanokristallen
Kashas-regel doorbreken:wetenschappers vinden unieke luminescentie in tetrapod-nanokristallen Wie heeft een astrolabe uitgevonden?
Wie heeft een astrolabe uitgevonden?  De wetenschap die zich bezighoudt met de vorm en structuur van plantendieren?
De wetenschap die zich bezighoudt met de vorm en structuur van plantendieren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

