
Wetenschap
Alkaliën begrijpen:waarom ze als basen worden beschouwd
1. Arrhenius-definitie:
* Basis: Volgens de definitie van Arrhenius is een base een stof die hydroxide-ionen (OH-) produceert wanneer deze in water wordt opgelost.
* Alkali: Een alkali is specifiek een oplosbare base , wat betekent dat het oplost in water en een oplossing vormt die hydroxide-ionen bevat.
2. Breder perspectief:
* Basis: De term "base" is breder dan "alkali" en omvat stoffen die protonen (H+) kunnen accepteren volgens de Brønsted-Lowry-theorie.
* Alkali: Deze term is in het algemeen beperkt tot hydroxidehoudende verbindingen die oplosbaar zijn in water.
Voorbeeld:
* NaOH (natriumhydroxide): Dit is zowel een alkali als een base. Het lost op in water om hydroxide-ionen (OH-) te vormen en wordt als een sterke base beschouwd.
* NH3 (Ammoniak): Dit is een base, maar geen alkali. Het accepteert protonen in water om ammoniumionen (NH4+) te vormen, maar het produceert niet direct hydroxide-ionen zoals alkalische stoffen dat doen.
Samengevat:
* Alkali is een subset van bases specifiek verwijzend naar oplosbare hydroxidebevattende verbindingen.
* De term 'base' omvat een breder scala aan stoffen die protonen kunnen accepteren.
Daarom is het juist om te zeggen "alkaliën zijn basen", omdat ze een specifiek type base zijn. Voor een alomvattend begrip is het echter belangrijk om de verschillen en bredere definities van 'base' en 'alkali' te begrijpen.
 Uitleggen waarom condensatie exotherm is
Uitleggen waarom condensatie exotherm is  Heeft gas een hoge dichtheid?
Heeft gas een hoge dichtheid?  Wat is de reactie wanneer kaliumacetaat in water wordt gestopt?
Wat is de reactie wanneer kaliumacetaat in water wordt gestopt?  Hoe is gedeeltelijk smelten het tegenovergestelde van fractionele kristallisatie?
Hoe is gedeeltelijk smelten het tegenovergestelde van fractionele kristallisatie?  Een aardappelkubus wordt in een beker gevuld met heet zout water en nog een koud water geplaatst?
Een aardappelkubus wordt in een beker gevuld met heet zout water en nog een koud water geplaatst?
 Na EPA-flip, een duw om schadelijke pesticiden te blokkeren
Na EPA-flip, een duw om schadelijke pesticiden te blokkeren Adoptie groene hemelwaterinfrastructuur stijgt na overstromingen
Adoptie groene hemelwaterinfrastructuur stijgt na overstromingen Arseen komt vaker voor in putten in de buurt van gebroken gesteente in het zuidoosten van Wisconsin
Arseen komt vaker voor in putten in de buurt van gebroken gesteente in het zuidoosten van Wisconsin Sociologen zorgen ervoor dat water van dichtbij en ver weg stroomt
Sociologen zorgen ervoor dat water van dichtbij en ver weg stroomt Wat zijn de top 10 moeilijkste bossen op aarde?
Wat zijn de top 10 moeilijkste bossen op aarde?
Hoofdlijnen
- Wat is de functie van cytoplasma in een root haarcel?
- Hoe laat vertakking zien hoe organismen gerelateerd zijn aan één anouther?
- Wat is de term voor ouderorganismen die zijn gekoppeld?
- Hoe de inheemse praktijk van goed vuur onze bossen kan helpen gedijen
- Wat zijn onuitgesproken genen?
- Wat zijn voorbeelden van traditionele biotechnologie?
- Wat doet een mitochochondrion in cel?
- Wat is een mini -orgel dat de cel helpt bij het uitvoeren van bepaalde functies?
- Welke wetenschappers bepaalden de structuur van DNA?
- Chemici ontwerpen mini-ecosystemen om de werking van medicijnen te testen

- Superspons belooft effectieve giftige opruiming van meren en meer

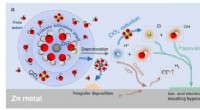
- Gehydrateerde eutectische elektrolyten helpen de prestaties van waterige zinkbatterijen te verbeteren
- Nieuw kathodemateriaal voor hoogwaardige natriumionbatterijen zou kunnen profiteren van grootschalige energieopslag

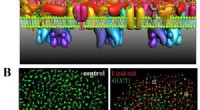
- Beeldvorming met superresolutie onthult het mechanisme van GLUT1-clustering
 Waarom is het menselijk lichaam verdeeld in systemen?
Waarom is het menselijk lichaam verdeeld in systemen?  Welke rol speelt het milieu in Darins -theorie van evolutie door natuurlijke selectie?
Welke rol speelt het milieu in Darins -theorie van evolutie door natuurlijke selectie?  Wanneer gameten combineren om een zygoot te vormen, wordt het aantal chromosomen nu nu aangeduid als?
Wanneer gameten combineren om een zygoot te vormen, wordt het aantal chromosomen nu nu aangeduid als?  Waarom wordt energie overgedragen van het ene molecuul naar het andere als twee zich bij verschillende temperaturen bevinden?
Waarom wordt energie overgedragen van het ene molecuul naar het andere als twee zich bij verschillende temperaturen bevinden?  Oceanische korst is wat dan continentale korst?
Oceanische korst is wat dan continentale korst?  Wat was de belangrijkste bron van brandstof voor energie in 1855?
Wat was de belangrijkste bron van brandstof voor energie in 1855?  Welk proces gebruikt zuurstof in plantenalgen en dieren?
Welk proces gebruikt zuurstof in plantenalgen en dieren?  Nieuwe synaptische architectuur voor op de hersenen geïnspireerd computergebruik
Nieuwe synaptische architectuur voor op de hersenen geïnspireerd computergebruik
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

