
Wetenschap
De elektronegativiteit van zuurstof in water:waarom het sterker is dan waterstof
Dit is waarom:
* Elektronegativiteit: Zuurstof is een veel elektronegatiever element dan waterstof. Elektronegativiteit is het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding. Zuurstof heeft een hogere elektronegativiteitswaarde dan waterstof, wat betekent dat het een sterkere aantrekkingskracht heeft op gedeelde elektronen.
* Polaire covalente binding: In water (H₂O) trekt het zuurstofatoom de gedeelde elektronen in de covalente bindingen met de waterstofatomen sterker aan. Hierdoor ontstaat een gedeeltelijke negatieve lading op het zuurstofatoom en gedeeltelijke positieve lading op de waterstofatomen. Dit maakt het watermolecuul een polair molecuul.
Samengevat: Het zuurstofatoom in watermoleculen trekt elektronen sterker aan dan de waterstofatomen vanwege de hogere elektronegativiteit.
 Verlies van Arctisch zee-ijs leidt tot frequentere sterke El Niño-gebeurtenissen
Verlies van Arctisch zee-ijs leidt tot frequentere sterke El Niño-gebeurtenissen Wetenschappers maken 's werelds eerste 3D-warmtebeeld van vulkaan
Wetenschappers maken 's werelds eerste 3D-warmtebeeld van vulkaan NASA-NOAA's Suomi NPP-satelliet vangt tyfoon Yutu-versterking, Guam op scherp
NASA-NOAA's Suomi NPP-satelliet vangt tyfoon Yutu-versterking, Guam op scherp NASA Terra Satellite onderzoekt het verplaatste centrum van Tropical Storm Hernans
NASA Terra Satellite onderzoekt het verplaatste centrum van Tropical Storm Hernans Bladeren, stam en wortels:genetici onthullen hoe een boom weet te groeien
Bladeren, stam en wortels:genetici onthullen hoe een boom weet te groeien
Hoofdlijnen
- Waarom zou een cel fotosynthese en ademhaling moeten doen?
- Waarom begint de biologische organisatie met submicroscopisch niveau?
- Welke cellulaire structuur in een dierlijke cel helpt homeostase te behouden door het transport van stoffen in en uit cel te regelen?
- Zijn vooral belangrijk in genetisch onderzoek dat de focus is van gedragsgenetica?
- Vrouwelijke reproductieve gezondheid begrijpen:een uitgebreid overzicht
- Onderzoekers ontcijferen hoe een enzym het genetisch materiaal in de celkern wijzigt
- Wat is de belangrijkste producent van bloedcellen?
- Wat zijn voorbeelden van kunstmatige actieve immuniteit?
- Vat de hiërarchie van de organisatie samen in complexe meercellige organismen samen?
- Wetenschappers ontwerpen organische kathode voor hoogwaardige batterijen

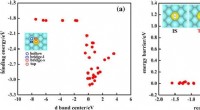
- AI zocht naar single-atom-alloy katalysatoren, 200 veelbelovende kandidaten gevonden
- De toekomst van zuivering verbeteren door moleculair silhouet te gebruiken om verbindingen in vloeistoffen te scheiden

- Onderzoekers vinden veelbelovende kandidaten voor nanodeeltjes voor het afvangen en omzetten van koolstofdioxide

- Hoe u nauwkeurig de pH van een mengsel van twee chemicaliën kunt berekenen

 Wat is een tak van de wetenschap die water of andere vloeistof in beweging behandelt?
Wat is een tak van de wetenschap die water of andere vloeistof in beweging behandelt?  Mest glipt door (bodem)scheuren
Mest glipt door (bodem)scheuren Een gasvormige verbinding is 78,14 procent boor en 21,86 procent?
Een gasvormige verbinding is 78,14 procent boor en 21,86 procent?  Online romantiek is lokaal, maar niet alle locaties zijn hetzelfde:studeren
Online romantiek is lokaal, maar niet alle locaties zijn hetzelfde:studeren Zullen zonnepanelen efficiënt zijn voor uw huis?
Zullen zonnepanelen efficiënt zijn voor uw huis?  Wat is de netto ionische vergelijking voor de reactie van hypochloor zuur en ammoniak?
Wat is de netto ionische vergelijking voor de reactie van hypochloor zuur en ammoniak?  Wat zijn de primaire mineralen die verloren zijn wanneer iemand transpireert?
Wat zijn de primaire mineralen die verloren zijn wanneer iemand transpireert?  Welk deel van een cel zou je bestuderen als je chromosomen wilde observeren?
Welk deel van een cel zou je bestuderen als je chromosomen wilde observeren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

