
Wetenschap
Verdampingswarmte:waarom diethylether minder energie vereist dan ethanol
1. Intermoleculaire krachten:
* Ethanol (CH3CH2OH): Ethanol vormt waterstofbruggen. Dit zijn sterke intermoleculaire krachten doordat het waterstofatoom direct gebonden is aan een zuurstofatoom. Waterstofbruggen vereisen een aanzienlijke hoeveelheid energie om te breken, wat leidt tot een hogere verdampingsenthalpie.
* Diethylether (CH3CH2OCH2CH3): Diethylether ervaart voornamelijk dipool-dipoolinteracties en Londense dispersiekrachten. Deze zijn zwakker dan waterstofbruggen.
2. Moleculaire structuur:
* Ethanol: De aanwezigheid van de hydroxylgroep (-OH) in ethanol maakt waterstofbinding mogelijk, wat bijdraagt aan het hogere kookpunt en de verdampingsenthalpie.
* Diethylether: De functionele ethergroep (R-O-R) mist het waterstofbruggende vermogen dat aanwezig is in ethanol.
3. Enthalpie van verdamping:
De verdampingsenthalpie is de hoeveelheid energie die nodig is om één mol van een stof bij het kookpunt te verdampen. Omdat diethylether zwakkere intermoleculaire krachten ervaart, is er minder energie nodig om deze interacties te verbreken en de moleculen van vloeistof naar gas over te zetten.
Samengevat:
De zwakkere intermoleculaire krachten in diethylether, vergeleken met de sterke waterstofbinding in ethanol, resulteren in een lagere verdampingsenthalpie. Dit betekent dat er minder warmte nodig is om diethylether te verdampen dan ethanol.
 Wat is de chemische verbinding gevormd tussen lithium en zwavel?
Wat is de chemische verbinding gevormd tussen lithium en zwavel?  Is het een goede strategie om chemische vergelijkingen in evenwicht te brengen?
Is het een goede strategie om chemische vergelijkingen in evenwicht te brengen?  Technieken voor het verlagen van het suikergehalte in zuivelproducten zijn veelbelovend
Technieken voor het verlagen van het suikergehalte in zuivelproducten zijn veelbelovend Voedingswetenschappers willen plantaardige eiwitten lekkerder en gezonder maken
Voedingswetenschappers willen plantaardige eiwitten lekkerder en gezonder maken Wat voor kracht werkt binnen een molecuul?
Wat voor kracht werkt binnen een molecuul?
 Gebied van aquatische omgeving waar licht kan doordringen?
Gebied van aquatische omgeving waar licht kan doordringen?  Is het waarschijnlijker dat op technologie gebaseerde intelligentie zich op het land of in het water zal ontwikkelen?
Is het waarschijnlijker dat op technologie gebaseerde intelligentie zich op het land of in het water zal ontwikkelen?  NASA vindt zware regenbuien in orkaan Bud
NASA vindt zware regenbuien in orkaan Bud Kopers van woningverzekeringen hebben geen toegang tot openbare gegevens over overstromingen
Kopers van woningverzekeringen hebben geen toegang tot openbare gegevens over overstromingen Opinie:Geen poot om op te staan – waarom de VS haar standpunt over herstelbetalingen voor het klimaat moeten heroverwegen
Opinie:Geen poot om op te staan – waarom de VS haar standpunt over herstelbetalingen voor het klimaat moeten heroverwegen
Hoofdlijnen
- Welke term is het beste van toepassing op al het materiaal in dit weefsel dat niet cellulair is?
- Wanneer werden cellen uitgevonden?
- Wat zijn de functies van een levercel?
- Welke organen zijn aan uw recht?
- Wat is het verschil tussen sporenmakers en zaadmakers?
- Waarom zijn bacteriën in de laatste stap van een voedselketen?
- Wat is een fysieke uitdrukking van genen?
- Chinese fruitvlieggenomen onthullen mondiale migraties en herhaalde evolutie
- Energiestroom (ecosysteem): definitie, proces en voorbeelden (met diagram)
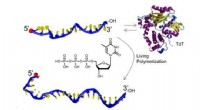
- Oddball-enzym biedt gemakkelijke weg naar synthetische biomaterialen
- Warmtefluxberekening:een praktische technische gids

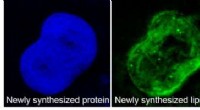
- De innerlijke werking van een levende cel in kaart brengen
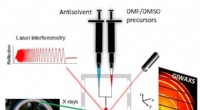
- Röntgenstralen onthullen in situ kristalgroei van loodvrije perovskiet-zonnepaneelmaterialen
- Reactanten versus producten:hun rol in chemische reacties begrijpen

 Hoe een paar geothermische centrales de Amerikaanse lithiumvoorzieningscrisis kunnen oplossen en de EV-batterijindustrie een boost kunnen geven
Hoe een paar geothermische centrales de Amerikaanse lithiumvoorzieningscrisis kunnen oplossen en de EV-batterijindustrie een boost kunnen geven Formule-eenheden van AgNO3 berekenen:een stapsgewijze handleiding
Formule-eenheden van AgNO3 berekenen:een stapsgewijze handleiding  Ontdekking onthult hoe bacteriën schadelijke en nuttige virussen onderscheiden
Ontdekking onthult hoe bacteriën schadelijke en nuttige virussen onderscheiden  Wat houdt de twee strengen DNA -moleculen bij elkaar?
Wat houdt de twee strengen DNA -moleculen bij elkaar?  Is mijn hond te koud? Hoe koud is te koud om te wandelen? Zo herken je
Is mijn hond te koud? Hoe koud is te koud om te wandelen? Zo herken je Met welk molecuul begint cellulaire ademhaling?
Met welk molecuul begint cellulaire ademhaling?  Kunnen genetica de vorm van een plant veranderen?
Kunnen genetica de vorm van een plant veranderen?  Luisteren huishoudens als de Fed een nieuwe monetaire-beleidsstrategie aankondigt?
Luisteren huishoudens als de Fed een nieuwe monetaire-beleidsstrategie aankondigt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

