
Wetenschap
Oplosbaarheid van ionische bindingen in water:een uitgebreide uitleg
* Polariteit: Watermoleculen zijn polair, wat betekent dat ze een positief uiteinde (waterstof) en een negatief uiteinde (zuurstof) hebben. Hierdoor kunnen watermoleculen ionen omringen en uit elkaar trekken.
* Elektrostatische interacties: Het positieve uiteinde van een watermolecuul kan het negatieve ion aantrekken, terwijl het negatieve uiteinde het positieve ion kan aantrekken. Dit verzwakt de elektrostatische aantrekkingskracht tussen de ionen in de ionische verbinding, wat leidt tot oplossing.
Er zijn echter uitzonderingen:
* Roosterenergie: Sommige ionische verbindingen hebben een zeer sterke elektrostatische aantrekkingskracht (hoge roosterenergie). Deze verbindingen lossen mogelijk niet gemakkelijk op in water. Calciumcarbonaat (CaCO3) is bijvoorbeeld slechts in geringe mate oplosbaar in water.
* Hydratie-energie: De energie die vrijkomt wanneer ionen worden omringd door watermoleculen (hydratatie-energie) moet voldoende zijn om de roosterenergie te overwinnen voordat oplossing plaatsvindt.
* Gemeenschappelijk ioneneffect: Als de oplossing al een hoge concentratie van één van de ionen uit de ionische verbinding bevat, zal de oplosbaarheid van de verbinding afnemen.
Samengevat: De meeste ionische verbindingen zijn oplosbaar in water vanwege de polaire aard van water en de elektrostatische interacties tussen watermoleculen en de ionen. Factoren zoals roosterenergie, hydratatie-energie en het gemeenschappelijke ioneneffect kunnen echter de oplosbaarheid beïnvloeden.
 Diep onder de oceaan, microben zijn actief en staan klaar om te eten wat er ook maar op hun pad komt
Diep onder de oceaan, microben zijn actief en staan klaar om te eten wat er ook maar op hun pad komt De Noord-Amerikaanse hittegolf laat zien dat we moeten weten hoe klimaatverandering ons weer zal veranderen
De Noord-Amerikaanse hittegolf laat zien dat we moeten weten hoe klimaatverandering ons weer zal veranderen Omnivoren die leven in de toendra
Omnivoren die leven in de toendra Zeehonden versus Walruses
Zeehonden versus Walruses  China's recyclingverbod roept op tot heroverweging op lange termijn in Australië
China's recyclingverbod roept op tot heroverweging op lange termijn in Australië
Hoofdlijnen
- Als een organisme kan groeien op zowel een voedingsagar- als MacConkey -agar, wat zou je dan beter verwachten?
- Zijn plantencellen eencellig of meercellulair?
- Waarom veranderen wetenschapper soms hun ideeën over het classificeren van organismen?
- Wat in een koelkast voorkomt dat bacteriën en schimmels op het eten komen?
- Wat zijn de drie variabelen in een wetenschappelijk experiment?
- Een amoeba bestaat uit een enkele cel en heeft kern. Hoe heet je?
- Hoe draagt geografische isolatie bij aan de evolutie van een nieuwe soort?
- Onderzoekers laten zien hoe voedselkeuze voor insecten kan worden gemanipuleerd
- Chili-pinguïns winnen slag in oorlog tegen de mijne
- Van flatscreen-tv's tot uw smartphone:het element borium verdient meer aandacht

- Een nieuwe manier om met zonlicht schone waterstofbrandstof te maken uit water

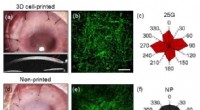
- 3D-geprinte kunstmatige hoornvliezen vergelijkbaar met menselijke hoornvliezen
- Onderzoekers ontwikkelen taaie, zelfherstellend rubber

- Bepaling van de optimale temperatuur voor enzymactiviteit

 Beeldvorming met hoge resolutie geeft een ongeëvenaard beeld van hoe schimmels groeien
Beeldvorming met hoge resolutie geeft een ongeëvenaard beeld van hoe schimmels groeien  Hoeveel stikstofatomen zijn er in ammoniumcarbonaat?
Hoeveel stikstofatomen zijn er in ammoniumcarbonaat?  Welke meeteenheid vertegenwoordigt het afstandslicht dat in één jaar lichtjaar of parsec reist?
Welke meeteenheid vertegenwoordigt het afstandslicht dat in één jaar lichtjaar of parsec reist?  Dagelijkse regenval boven Sumatra gekoppeld aan groter atmosferisch fenomeen
Dagelijkse regenval boven Sumatra gekoppeld aan groter atmosferisch fenomeen Wat zijn de vier sterrenstelsels?
Wat zijn de vier sterrenstelsels?  Welke eenheid is het beste om de dichtheid van een vaste stof uit te drukken?
Welke eenheid is het beste om de dichtheid van een vaste stof uit te drukken?  Een veranderende platina-elektrode observeren
Een veranderende platina-elektrode observeren Wat is de energie -input en output waar gaat naar voor persoon die een vuvuzela blaast?
Wat is de energie -input en output waar gaat naar voor persoon die een vuvuzela blaast?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

