
Wetenschap
Fluor's periodieke tabelbuurman:ontdek de overeenkomsten van chloor
Dit is waarom:
* Het zijn beide halogenen: Ze behoren tot groep 17 (VIIA) van het periodiek systeem, ook bekend als de halogenen.
* Vergelijkbare elektronegativiteit: Zowel fluor als chloor hebben een zeer hoge elektronegativiteit, wat betekent dat ze sterk elektronen aantrekken.
* Reactieve niet-metalen: Het zijn beide zeer reactieve niet-metalen die gemakkelijk negatieve ionen (anionen) vormen.
* Vergelijkbare hechtingseigenschappen: Ze hebben de neiging om enkele covalente bindingen met andere elementen te vormen.
Er zijn echter enkele verschillen tussen de twee:
* Fluor is het meest elektronegatieve element: Het heeft een hogere elektronegativiteit dan chloor.
* Reactiviteit: Fluor is over het algemeen reactiever dan chloor.
* Atoomgrootte: Chloor is groter dan fluor.
Over het algemeen delen fluor en chloor, vanwege hun vergelijkbare elektronenconfiguraties en positie in het periodiek systeem, veel belangrijke eigenschappen.
 Wanneer alle groep IIA hun valentie -elektronen verliezen, zijn de resterende configuraties hetzelfde als voor welke elementenfamilie?
Wanneer alle groep IIA hun valentie -elektronen verliezen, zijn de resterende configuraties hetzelfde als voor welke elementenfamilie?  Ontdek hoe cocaïne werkt
Ontdek hoe cocaïne werkt  Video:Wat is er nodig om de haven van Boston in thee te veranderen?
Video:Wat is er nodig om de haven van Boston in thee te veranderen? Geef de elektronenconfiguratie voor een neutraal atoom van chloor?
Geef de elektronenconfiguratie voor een neutraal atoom van chloor?  Hoe een gunstige darmmicrobe zich aanpaste aan moedermelk
Hoe een gunstige darmmicrobe zich aanpaste aan moedermelk
 Wetenschapsrapport:Wie wordt heter, natter met klimaatverandering
Wetenschapsrapport:Wie wordt heter, natter met klimaatverandering Nieuwe methode voor massaproductie van recombinante eiwitten maakt gebruik van mononatriumglutamaat
Nieuwe methode voor massaproductie van recombinante eiwitten maakt gebruik van mononatriumglutamaat  'Hoe ruiken oude boeken?' – Het behoud van geuren als belangrijk cultureel erfgoed
'Hoe ruiken oude boeken?' – Het behoud van geuren als belangrijk cultureel erfgoed  Carbon Cycling in Aquatic Ecosystems
Carbon Cycling in Aquatic Ecosystems  Wetenschappers laten zien dat planten de kortste dag kunnen meten
Wetenschappers laten zien dat planten de kortste dag kunnen meten
Hoofdlijnen
- Welke organel zou je verwachten in plantencellen maar geen dierlijke cellen?
- Wat zijn de 4 verschillende bases in DNA?
- Welk molecuul voltooit de informatiestroom van DNA naar eiwit?
- Welke soorten biomen zijn er in Azerbeidzjan?
- Welke abiotische factor beïnvloedt de paddenstoel?
- Welke structuren hebben plantencellen?
- High-tech tools onthullen opalen fossiel skelet
- Is een Liana een dier of plant?
- Welke vorm zijn dierencellen?
- Nieuwe aanpak kan leiden tot ontworpen kunststoffen met specifieke eigenschappen

- Wat als we krachtige medicijnen zouden kunnen ontwerpen zonder ongewenste bijwerkingen?

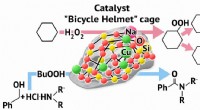
- Chemicus ontwikkelt nieuwe katalysator voor oxidatie en amidering
- Ontdekking van een nieuwe wet van fasescheiding

- Robotchemicus ontdekt nieuwe moleculen en reacties

 Hoe heette de space shuttle die betrokken was bij de eerste maanlanding?
Hoe heette de space shuttle die betrokken was bij de eerste maanlanding?  Wat geeft katalyse een voorbeeld?
Wat geeft katalyse een voorbeeld?  Wat is een mengsel van koolwaterstoffen die voorkomen met petroleumafzettingen?
Wat is een mengsel van koolwaterstoffen die voorkomen met petroleumafzettingen?  Drop the donut:ware aard van verhongerde superzware zwarte gaten onthuld
Drop the donut:ware aard van verhongerde superzware zwarte gaten onthuld  Wat is een homologe eigenschap?
Wat is een homologe eigenschap?  Als drones de nacht verlichten, zullen ze dan vuurwerk vervangen?
Als drones de nacht verlichten, zullen ze dan vuurwerk vervangen?  Zijn er dieren zonder cellen?
Zijn er dieren zonder cellen?  3 breuken vermenigvuldigen
3 breuken vermenigvuldigen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

