
Wetenschap
Hydrofiele opgeloste stoffen begrijpen:eigenschappen en voorbeelden
Hier is een overzicht:
* Polariteit: Water is een polair molecuul, wat betekent dat het een positief uiteinde en een negatief uiteinde heeft. Hierdoor kan het sterke bindingen vormen met andere polaire moleculen.
* Hydrofiele opgeloste stoffen: Deze opgeloste stoffen zijn ook polair en bevatten geladen groepen of polaire functionele groepen zoals hydroxyl- (-OH), carboxyl- (-COOH) of amine- (-NH2) groepen. Deze groepen kunnen waterstofbruggen vormen met water, waardoor ze gemakkelijk oplosbaar worden.
Voorbeelden van hydrofiele opgeloste stoffen zijn:
* Suikers: Glucose, fructose, sucrose
* Zouten: Natriumchloride (NaCl)
* Zuren: Citroenzuur, azijnzuur
* Alcoholen: Ethanol, methanol
* Aminozuren: De bouwstenen van eiwitten
In tegenstelling daarmee:
* Hydrofobe opgeloste stoffen zijn niet-polair en lossen niet gemakkelijk op in water. Ze worden aangetrokken door andere niet-polaire moleculen en hebben de neiging samen te klonteren in water. Voorbeelden zijn onder meer vetten, oliën en wassen.
 Hoe onze bossen zich aanpassen aan klimaatverandering
Hoe onze bossen zich aanpassen aan klimaatverandering Palmolie moet duurzamer worden gemaakt, terwijl vervangingen schaalbaar moeten worden gemaakt, ingenieurs waarschuwen
Palmolie moet duurzamer worden gemaakt, terwijl vervangingen schaalbaar moeten worden gemaakt, ingenieurs waarschuwen Welke invloed heeft ontbossing op de zuurstof?
Welke invloed heeft ontbossing op de zuurstof?  Is rundvlees de nieuwe steenkool? Klimaatvriendelijk eten zit in de lift
Is rundvlees de nieuwe steenkool? Klimaatvriendelijk eten zit in de lift Kunnen woestijnsteden als Tucson en Phoenix waterbronnen duurzaam maken?
Kunnen woestijnsteden als Tucson en Phoenix waterbronnen duurzaam maken?
Hoofdlijnen
- Een DNA-model maken met piepschuimballen
- Hoe bacteriën worden geclassificeerd op de bases van flagella?
- Wat bevat een DNA -nucleotide?
- Metabolisme uitgelegd:een eenvoudige definitie en overzicht
- Waar behouden protisten hun DNA?
- Hoe heet de moderne versie van prokaryote cellen?
- Meristematische cellen die de add -breedte worden genoemd om lichaam te planten?
- Wat zijn de vijf niveaus van biologische organisatie binnen een organisme?
- Wat zou er gebeuren als de kern nooit zou bestaan?
- Wegenkaart schetst hindernissen bij de ontwikkeling van kathodes van de volgende generatie voor het aandrijven van elektrische voertuigen
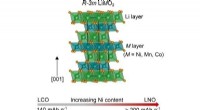
- Nieuwe materialen in de magnetron

- Op groene fluorescerende eiwitten gebaseerde glucose-indicatoren voor realtime monitoring van het glucosemetabolisme
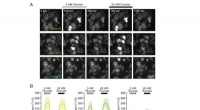
- Hoe mosselen hun hechting onder water behouden
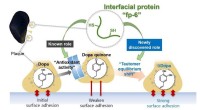
- Het bereiken van stabiele K-opslagprestaties van met koolstofbolletjes opgesloten antimoon via elektrolytregulatie
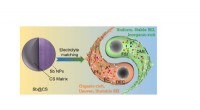
 De oudste objecten in het zonnestelsel waarvan de leeftijd is gemeten, zijn?
De oudste objecten in het zonnestelsel waarvan de leeftijd is gemeten, zijn?  Intra-rij onkruid wieden mogelijk met vision-systemen
Intra-rij onkruid wieden mogelijk met vision-systemen NASA's WFIRST zal helpen het lot van het universum te ontdekken
NASA's WFIRST zal helpen het lot van het universum te ontdekken Wat is de breedtegraad en lengtegraad van Constellation Perseus?
Wat is de breedtegraad en lengtegraad van Constellation Perseus?  AI om te bepalen wanneer u moet ingrijpen bij uw rijgedrag
AI om te bepalen wanneer u moet ingrijpen bij uw rijgedrag Fatsoenlijk leven voor iedereen hoeft de aarde niet te kosten
Fatsoenlijk leven voor iedereen hoeft de aarde niet te kosten Hoe laat begint de zon onder te gaan?
Hoe laat begint de zon onder te gaan?  Hellingen zoeken
Hellingen zoeken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

