
Wetenschap
Rubidium-reactiviteit:de hoge reactiviteit ervan begrijpen
* Lage ionisatie-energie: Het verliest gemakkelijk zijn buitenste elektron en wordt een positief geladen ion (Rb+). Dit gemak van ionisatie maakt het zeer reactief, vooral met niet-metalen.
* Grote atoomstraal: De grote atoomstraal van Rubidium betekent dat het buitenste elektron zich ver van de kern bevindt en minder stevig wordt vastgehouden, waardoor het gemakkelijk verloren gaat.
* Elektropositieve aard: Rubidium is zeer elektropositief, wat betekent dat het een sterke neiging heeft om elektronen te verliezen en positieve ionen te vormen.
Zo ziet de reactiviteit ervan eruit:
* Reactie met lucht: Rubidium reageert explosief met lucht, ontbrandt spontaan en vormt rubidiumoxide.
* Reactie met water: Het reageert heftig met water, waarbij waterstofgas vrijkomt en warmte ontstaat die de waterstof kan ontsteken, waardoor een explosie ontstaat.
* Reactie met halogenen: Rubidium reageert krachtig met halogenen (zoals chloor, broom en jodium) om rubidiumhalogeniden te vormen.
* Reactie met zuren: Rubidium reageert explosief met zuren, waarbij waterstofgas ontstaat.
Behandeling en opslag:
Vanwege zijn extreme reactiviteit wordt rubidium opgeslagen onder inerte atmosferen zoals argon of in minerale olie om contact met lucht en vocht te voorkomen. Het vereist een zorgvuldige behandeling in een laboratoriumomgeving om ongelukken te voorkomen.
Toepassingen:
Ondanks zijn reactiviteit heeft rubidium nichetoepassingen:
* Atoomklokken: De spectrale eigenschappen van Rubidium worden gebruikt in atoomklokken, die bekend staan om hun hoge precisie.
* Fotocellen: Rubidium wordt in sommige soorten fotocellen gebruikt.
* Onderzoek: Gebruikt in verschillende onderzoeksgebieden, waaronder scheikunde en natuurkunde.
Samengevat: Rubidium is een zeer reactief alkalimetaal dat explosief reageert met lucht, water en vele andere stoffen. De reactiviteit komt voort uit de lage ionisatie-energie, de grote atoomstraal en het elektropositieve karakter. Hoewel het gevaarlijk is om ermee om te gaan, wordt het vanwege zijn unieke eigenschappen op specifieke gebieden toegepast.
 Wat zijn voorbeeld van een hydroxylgroep?
Wat zijn voorbeeld van een hydroxylgroep?  Platina en waterstofperoxide:katalytische ontleding uitgelegd
Platina en waterstofperoxide:katalytische ontleding uitgelegd  Nieuw productieproces creëert superkleine kanalen om water af te weren en medische, elektronische apparaten
Nieuw productieproces creëert superkleine kanalen om water af te weren en medische, elektronische apparaten Hoe u een team van 'passend sceptische' accountants van financiële overzichten kunt samenstellen
Hoe u een team van 'passend sceptische' accountants van financiële overzichten kunt samenstellen  Hoe scheid je ammoniak en waterstof?
Hoe scheid je ammoniak en waterstof?
 Orkaan Iota nu een storm van categorie 5 nabij Midden-Amerika
Orkaan Iota nu een storm van categorie 5 nabij Midden-Amerika Het plantenleven breidt zich uit in de Everest-regio
Het plantenleven breidt zich uit in de Everest-regio Is er een technologische oplossing voor aquatische dode zones?
Is er een technologische oplossing voor aquatische dode zones? Geef de shiraz door, alsjeblieft:hoe de Australische wijnindustrie zich kan aanpassen aan klimaatverandering
Geef de shiraz door, alsjeblieft:hoe de Australische wijnindustrie zich kan aanpassen aan klimaatverandering De combinatie van waterschaarste en een starre vraag brengt de stroomgebieden van de wereld in gevaar
De combinatie van waterschaarste en een starre vraag brengt de stroomgebieden van de wereld in gevaar
Hoofdlijnen
- Welke factoren zijn de soorten organismen die in een zoutwaterecosysteem kunnen leven?
- Klier die een factor scheidt, zorgt ervoor dat T-cellen volwassen worden?
- Welk membraan bestaat volledig uit bindweefsel?
- Wat is het belangrijkste resultaat van fotosynthese?
- Welke organellen vormen koolhydraten in planten?
- Wat is het proces van het verkrijgen van kwantitatieve informatie over verschillende fenomenen?
- Welke karakteristieken maken Euglenophytes anders dan andere protisten?
- Wat beschrijft een enzym nauwkeurig?
- Welk weefsel heeft weinig tot geen functionele regeneratiecapaciteit?
- Wetenschappers gebruiken nanotechnologie om de prestaties van belangrijke industriële katalysatoren te verbeteren

- Supramoleculaire complexvorming - antraceen macrocyclus en C60 fullereen

- Onderzoekers ontdekken proces om psilocybine duurzaam te produceren een kandidaat-geneesmiddel dat kan helpen bij de behandeling van depressie

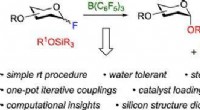
- Suikers synthetiseren:scheikundigen ontwikkelen methode om de opbouw van koolhydraten te vereenvoudigen
- Blootstelling aan ultraviolet licht verbetert het beschermende vermogen van synthetische melanine

 Airconditioning in een veranderend klimaat:een groeiende kloof tussen rijk en arm
Airconditioning in een veranderend klimaat:een groeiende kloof tussen rijk en arm Een ultra-rekbare tribo-elektrische stripsensor (TSS) om objecten in 3D-ruimte te besturen
Een ultra-rekbare tribo-elektrische stripsensor (TSS) om objecten in 3D-ruimte te besturen Darmkanker en doodgeboorten voorkomen
Darmkanker en doodgeboorten voorkomen Een materiaal dat de meeste vloeistoffen niet nat maken
Een materiaal dat de meeste vloeistoffen niet nat maken Welke planeet heeft het meeste van de sateliet?
Welke planeet heeft het meeste van de sateliet?  Hoeveel chloor atomen zullen waarschijnlijk combineren met fosfor?
Hoeveel chloor atomen zullen waarschijnlijk combineren met fosfor?  Wat gebeurt er met potentiële energie wanneer een proton dichter bij een elektron wordt gebracht?
Wat gebeurt er met potentiële energie wanneer een proton dichter bij een elektron wordt gebracht?  Welke warmte is de hoeveelheid thermische energie die nodig is om de temperatuur één kilogram een stof met 1 graden Celsius te verhogen?
Welke warmte is de hoeveelheid thermische energie die nodig is om de temperatuur één kilogram een stof met 1 graden Celsius te verhogen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

