
Wetenschap
Polaire verbindingen:inzicht in elektronegativiteit en moleculaire polariteit
Hier is een overzicht:
* Elektronegativiteit: Dit is het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding. Verschillende elementen hebben verschillende elektronegativiteiten.
* Polaire covalente binding: Wanneer twee atomen met verschillende elektronegativiteiten een binding vormen, worden de elektronen meer naar het atoom met een hogere elektronegativiteit getrokken. Hierdoor ontstaat een gedeeltelijke negatieve lading (δ-) op het meer elektronegatieve atoom en een gedeeltelijke positieve lading (δ+) op het minder elektronegatieve atoom.
* Polair molecuul: Als een molecuul polaire covalente bindingen heeft en de bindingen asymmetrisch zijn gerangschikt, zal het molecuul een netto dipoolmoment hebben, wat betekent dat het een positief en een negatief uiteinde zal hebben.
Eigenschappen van polaire verbindingen:
* Oplosbaarheid in water: Polaire verbindingen hebben de neiging om in water op te lossen, omdat water ook een polair molecuul is. Het positieve uiteinde van het watermolecuul kan het negatieve uiteinde van de polaire verbinding aantrekken, en omgekeerd.
* Hoge kookpunten: Polaire verbindingen hebben doorgaans hogere kookpunten dan niet-polaire verbindingen, omdat de intermoleculaire krachten tussen polaire moleculen sterker zijn.
* Goede elektriciteitsgeleiders: Wanneer opgelost in water kunnen polaire verbindingen elektriciteit geleiden omdat de geladen ionen vrij kunnen bewegen.
Voorbeelden van polaire verbindingen:
* Water (H₂O): Het zuurstofatoom is elektronegatiever dan de waterstofatomen, wat resulteert in een polair molecuul.
* Ethanol (C₂H₅OH): Het zuurstofatoom in de hydroxylgroep (OH) is elektronegatiever dan de koolstof- en waterstofatomen.
* Waterstofchloride (HCl): Chloor is elektronegatiever dan waterstof, waardoor het molecuul polair is.
In tegenstelling tot niet-polaire verbindingen hebben een gelijkmatige verdeling van elektronen en hebben geen positief of negatief uiteinde. Ze hebben doorgaans lage kookpunten en zijn niet oplosbaar in water. Voorbeelden hiervan zijn methaan (CH₄) en olie.
 Wat zijn de beschuldigingen op natriumion en chloride nadat ze gecombineerd zijn?
Wat zijn de beschuldigingen op natriumion en chloride nadat ze gecombineerd zijn?  Hoe wordt het genoemd als stikstof gecombineerd met andere elementen?
Hoe wordt het genoemd als stikstof gecombineerd met andere elementen?  Loodhalogenide perovskieten met verbeterde luminescentie en stabiliteit
Loodhalogenide perovskieten met verbeterde luminescentie en stabiliteit Wat zijn stabiele elementen?
Wat zijn stabiele elementen?  Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van initiële concentraties
Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van initiële concentraties
 Wat zijn Consmers in een ecosysteem?
Wat zijn Consmers in een ecosysteem?  Wat zijn de verschillende soorten land?
Wat zijn de verschillende soorten land?  Welk organisme dat een bos in het zuidoosten van de Verenigde Staten kan bezetten?
Welk organisme dat een bos in het zuidoosten van de Verenigde Staten kan bezetten?  Een worp met de dobbelstenen:onderzoekers uit de kwantummechanica laten zien dat de natuur onvoorspelbaar is
Een worp met de dobbelstenen:onderzoekers uit de kwantummechanica laten zien dat de natuur onvoorspelbaar is  Hoe zit het met de recente wilde tornado's? Deskundige weegt mee
Hoe zit het met de recente wilde tornado's? Deskundige weegt mee
Hoofdlijnen
- Wat is een bioprospecteur?
- Hoe werden de nieuwe cellen gevormd uit de meiose vergeleken met elkaar?
- Wat moet u vinden over een prokaryote om te weten welk domein het behoort?
- Enkele cellen organismen met lange zweepachtige staarten?
- Wat reguleert de beweging van materialen in en uit de cel?
- Fruitvliegjesplaag ontmoet zijn evolutionaire match in sluipwesp
- Is uitsterven ooit een goede zaak?
- Welk orgaan vormen het immuunsysteem?
- Wat is het orgaan van reproductie in zulke bloeiende planten als Crocus en Gladiolus?
- Designer-eiwitten vormen draden en roosters op een mineraal oppervlak

- Wetenschappers gebruiken nanotechnologie om de prestaties van belangrijke industriële katalysatoren te verbeteren

- Een betere hiv-test

- De natuur biedt een sleutel tot het afstoten van vloeistoffen

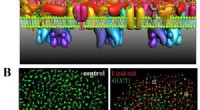
- Beeldvorming met superresolutie onthult het mechanisme van GLUT1-clustering
 De eerste orkaan van 2021 kwam vroeg. Het kan een teken zijn van wat komen gaat
De eerste orkaan van 2021 kwam vroeg. Het kan een teken zijn van wat komen gaat Akoestische golven geven een boost aan realtime seismische beeldvorming
Akoestische golven geven een boost aan realtime seismische beeldvorming Waarom verschillen mannen en vrouwen vaak in lichaamsgroottestructuur?
Waarom verschillen mannen en vrouwen vaak in lichaamsgroottestructuur?  Het noordpoolgebied is in 3 miljoen jaar niet zo warm geweest – en dat voorspelt grote veranderingen voor de rest van de planeet
Het noordpoolgebied is in 3 miljoen jaar niet zo warm geweest – en dat voorspelt grote veranderingen voor de rest van de planeet Lancering:Antares-raket stimuleert bevoorradingsschip van Virginia naar het ruimtestation
Lancering:Antares-raket stimuleert bevoorradingsschip van Virginia naar het ruimtestation Moiré-effect:materiaaleigenschappen verdraaien
Moiré-effect:materiaaleigenschappen verdraaien  Welke doeleinden worden kolen vaak gebruikt?
Welke doeleinden worden kolen vaak gebruikt?  Waar krijgt op aarde de meeste zon?
Waar krijgt op aarde de meeste zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

