
Wetenschap
Inzicht in de instabiliteit van anti-aromatische verbindingen
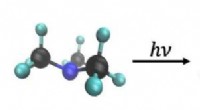
Anti-aromatische verbindingen
* Hoge energie: Anti-aromatische verbindingen hebben een cyclische, vlakke structuur met een continu π-systeem, maar ze bezitten 4n π-elektronen (waarbij n een geheel getal is). Dit specifieke aantal elektronen leidt tot een destabiliserende overtreding van de regel van Huckel . De elektronen in het π-systeem worden in een hogere energietoestand gedwongen, waardoor het molecuul minder stabiel is dan zijn niet-cyclische tegenhangers.
* Verhoogde afstoting: De π-elektronen in anti-aromatische verbindingen zijn beperkt tot een kleinere ruimte, waardoor de elektron-elektronenafstoting toeneemt en het molecuul verder wordt gedestabiliseerd.
* Gebrek aan resonantiestabilisatie: In tegenstelling tot aromatische verbindingen vertonen anti-aromatische verbindingen geen significante resonantiestabilisatie vanwege de ongunstige elektronenrangschikking.
Niet-aromatische verbindingen
* Gebrek aan vlakheid: Niet-aromatische verbindingen missen vaak de vlakke structuur die nodig is voor effectieve π-elektronendelokalisatie. Dit kan gebeuren als gevolg van de aanwezigheid van sp³-gehybridiseerde koolstofatomen in de ring, sterische spanning of de aanwezigheid van omvangrijke substituenten.
* Onvoldoende π-elektronenaantal: Niet-aromatische verbindingen bezitten mogelijk niet het specifieke aantal π-elektronen dat nodig is voor aromatiteit (4n + 2, waarbij n een geheel getal is). Dit resulteert in een gebrek aan cyclische π-elektronendelokalisatie en bijgevolg in een gebrek aan resonantiestabilisatie.
Voorbeelden
* Anti-aromatisch: Cyclobutadieen (4 π elektronen), cyclooctatetraeen (8 π elektronen)
* Niet-aromatisch: Cyclohexaan (geen π-elektronen), cyclopentaan (geen π-elektronen), cycloheptatrieen (6 π-elektronen maar niet vlak)
Samenvattend komt de instabiliteit van anti-aromatische verbindingen voort uit hun overtreding van de regel van Huckel, wat leidt tot hoge energie en verhoogde elektronenafstoting. Niet-aromatische verbindingen missen daarentegen de specifieke structurele vereisten voor aromatiteit, zoals vlakheid of een geschikt π-elektronenaantal, wat resulteert in verminderde stabiliteit.
 Wat als de VS stoppen met klimaatdeal? Ziet er niet goed uit voor de aarde
Wat als de VS stoppen met klimaatdeal? Ziet er niet goed uit voor de aarde Betere winterweersvoorspellingen voor luchthavens
Betere winterweersvoorspellingen voor luchthavens 'Onaangepastheid':hoe niet om te gaan met klimaatverandering
'Onaangepastheid':hoe niet om te gaan met klimaatverandering  De omvang van de grote aardbeving in Lissabon was mogelijk lager dan eerdere schattingen
De omvang van de grote aardbeving in Lissabon was mogelijk lager dan eerdere schattingen De manier waarop planten koolstof gebruiken, beïnvloedt hun reactie op klimaatverandering
De manier waarop planten koolstof gebruiken, beïnvloedt hun reactie op klimaatverandering
Hoofdlijnen
- Wat voor soort reproductie produceert organismen die verschillen van beide ouders?
- Wat zijn de twee soorten haploïde cellen gemaakt in meiose?
- Wat is de wetenschappelijke naam van Palisades -cel?
- Hoe reproduceren eukaryoten zich?
- Naam van het proces waar water plantencel verlaat?
- Is biopolair een aandoening waarmee u wordt geboren of wordt deze geërfd?
- Waar wordt Myelin gevonden en wat zijn functie?
- Nieuwe methode maakt bio-ethanol uit afval in bestaande installaties
- De hoeveelheid organisch materiaal dat de autotrofe organismen een ecosysteem produceren?
- Kijken hoe moleculen in realtime worden gesplitst
- Onderzoekers die werken aan het terugwinnen van zeldzame aardelementen en het veiligstellen van kritieke materialen voor schone energietechnologieën

- Spinazie gebruikt in neutronenstudies zou het geheim kunnen ontrafelen voor een sterkere plantengroei

- Meer zonne-energie dankzij titanium

- Hoe valentie-elektronen elementgroepen in het periodiek systeem bepalen
 Waar haalt de plant koolstof vandaan om structuren te maken?
Waar haalt de plant koolstof vandaan om structuren te maken?  Wat bevat een ziekteverwekker?
Wat bevat een ziekteverwekker?  Wat is een elastische kracht?
Wat is een elastische kracht?  Hoe het coronavirus de wereldwijde toeleveringsketen wel en niet heeft verstoord
Hoe het coronavirus de wereldwijde toeleveringsketen wel en niet heeft verstoord Wat zijn zes voordelen van windenergie?
Wat zijn zes voordelen van windenergie?  Het gebruik van AI uitbreiden via het internet der dingen
Het gebruik van AI uitbreiden via het internet der dingen Wat zijn vormen van energie geassocieerd met de deeltjes die objecten vormen?
Wat zijn vormen van energie geassocieerd met de deeltjes die objecten vormen?  Nieuwe uitvinding zorgt voor een revolutie in exoskeletten
Nieuwe uitvinding zorgt voor een revolutie in exoskeletten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

