
Wetenschap
Chloor:atoom versus ion - Chemische binding begrijpen
* Chlooratoom (Cl): Dit is de neutrale vorm van chloor en bevat 17 protonen en 17 elektronen. Het bestaat als een diatomisch molecuul (Cl₂) in zijn elementaire vorm.
* Chloorion (Cl⁻): Dit is een negatief geladen vorm van chloor, met 17 protonen en 18 elektronen. Het krijgt een extra elektron om een stabiele elektronenconfiguratie te bereiken, waardoor het een anion wordt.
Hoe je het verschil ziet:
* Kosten: Een chlooratoom heeft netto geen lading, terwijl een chloorion een negatieve lading heeft.
* Context: Als je te maken hebt met een molecuul of verbinding die chloor bevat, is het chloor waarschijnlijk een ion. In natriumchloride (NaCl) komt chloor bijvoorbeeld voor als Cl⁻.
* Chemische reacties: Chlooratomen kunnen tijdens chemische reacties elektronen winnen om chloride-ionen te vormen.
Samengevat: Chloor kan voorkomen als een neutraal atoom (Cl) of een negatief geladen ion (Cl⁻), afhankelijk van zijn toestand en betrokkenheid bij chemische reacties.
 Als een solide stuk naftaleen wordt verwarmd en op 80 graden Celsius blijft totdat het volledig is gesmolten, weet je dat dat is?
Als een solide stuk naftaleen wordt verwarmd en op 80 graden Celsius blijft totdat het volledig is gesmolten, weet je dat dat is?  NRL heeft patent verleend voor microbiële brandstofcel op zonne-energie
NRL heeft patent verleend voor microbiële brandstofcel op zonne-energie Wat is de molariteit van een oplossing die is bereid wanneer 75,0 ml 4,00 M KCl verdund tot volume 0,500 L?
Wat is de molariteit van een oplossing die is bereid wanneer 75,0 ml 4,00 M KCl verdund tot volume 0,500 L?  Waarom hebben planten water nodig in fotosynthese?
Waarom hebben planten water nodig in fotosynthese?  Welke factoren beïnvloeden het smeltpunt?
Welke factoren beïnvloeden het smeltpunt?
 Klimaatprojecties laten zien dat er binnen dertig jaar gevolgen voor de menselijke gezondheid kunnen zijn
Klimaatprojecties laten zien dat er binnen dertig jaar gevolgen voor de menselijke gezondheid kunnen zijn  Koude lucht stijgt op – wat dat betekent voor het klimaat op aarde
Koude lucht stijgt op – wat dat betekent voor het klimaat op aarde  Wat voorkomt dat water het beste verdampt in de categorie van milieuwetenschappen of aardwetenschappen?
Wat voorkomt dat water het beste verdampt in de categorie van milieuwetenschappen of aardwetenschappen?  Ondergrondse voedselbronnen stellen bacteriën in staat om arseen in het grondwater af te geven
Ondergrondse voedselbronnen stellen bacteriën in staat om arseen in het grondwater af te geven De bronnen van trans-Pacific stof opsporen
De bronnen van trans-Pacific stof opsporen
Hoofdlijnen
- Waarom zijn enzymen nodig om chemische reacties met cellen te regelen?
- Welke omstandigheden zou de enzymatische activiteit in een bacteriële cel verhogen die normaal gesproken het menselijk lichaam gedijt?
- Deze muizen worden groter aan de regenachtigere kanten van bergen:het kan een nieuwe regel van de natuur zijn
- Welke eiwitbevattende stoffen spelen een rol in de verdediging?
- Hoe hebben levende wezens aan elk bioom aangepast?
- Kunnen genetica de vorm van een plant veranderen?
- Wat is het DNA -segment van Ugauuc van mRNA?
- Onderzoek laat zien hoe de ineenstorting van eiwitprocessen veroudering en dood van de bestuurder veroorzaakt
- Wat zijn de celdelen die plantencellen onderscheiden van diercellen?
- Op hout gebaseerde vezels vangen hormonen uit afvalwater

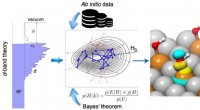
- De geheimen van chemische binding ontrafelen met machine learning
- Wetenschappers ontwikkelen een effectief systeem voor de levering van biomateriaal aan laboratoria

- Nieuwe methode biedt eerste blik op superkoude koolstofmoleculen

- Het mechanisme van metaalextractie met ionische vloeistoffen bestuderen
 Welke rol spelen eiwitten om de enorme hoeveelheid DNA een eukaryotische cel in kern te laten verlichten en hoe worden die genoemd?
Welke rol spelen eiwitten om de enorme hoeveelheid DNA een eukaryotische cel in kern te laten verlichten en hoe worden die genoemd?  Nieuwe technologie zal laten zien hoe RNA de genactiviteit reguleert
Nieuwe technologie zal laten zien hoe RNA de genactiviteit reguleert  Chemokinereceptor CX3CR1-structuren onthullen mechanisme van cholesterolregulatie bij activering
Chemokinereceptor CX3CR1-structuren onthullen mechanisme van cholesterolregulatie bij activering Wat zijn kenmerken van eukaryoot?
Wat zijn kenmerken van eukaryoot?  Welke kernenergie gebruikt de Verenigde Staten?
Welke kernenergie gebruikt de Verenigde Staten?  In een dierentuin gekweekte koralen hebben zich aangesloten bij het grootste rif van Europa. Dit biedt wetenschappers hoop
In een dierentuin gekweekte koralen hebben zich aangesloten bij het grootste rif van Europa. Dit biedt wetenschappers hoop  Wat zijn de bijdragen van Ramon C. Barba in de chemie?
Wat zijn de bijdragen van Ramon C. Barba in de chemie?  Is ATP de Universal Energy Carrier?
Is ATP de Universal Energy Carrier?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

