
Wetenschap
Natriumchloridevorming:de ionische binding begrijpen
1. Elektronische configuratie:
* Natrium heeft één elektron in de buitenste schil (valentie-elektron).
* Chloor heeft zeven elektronen in de buitenste schil.
2. De drang naar stabiliteit:
* Atomen streven naar een volledige buitenste schil van elektronen voor stabiliteit. Dit is de basis van de octetregel (behalve voor waterstof en helium die streven naar een duet, dat wil zeggen twee elektronen in hun buitenste schil).
3. Overdracht van elektronen:
* Natrium verliest gemakkelijk zijn enkele valentie-elektron en wordt een positief geladen ion (Na+).
* Chloor krijgt gemakkelijk één elektron om zijn buitenste schil te vullen en wordt een negatief geladen ion (Cl-).
4. Elektrostatische aantrekkingskracht:
* De tegengesteld geladen natrium- en chloride-ionen trekken elkaar aan door elektrostatische krachten, waardoor een ionische binding ontstaat. Deze aantrekkingskracht houdt de ionen bij elkaar in een kristalroosterstructuur.
5. Vorming van natriumchloride (NaCl):
* De sterke elektrostatische aantrekkingskracht tussen Na+ en Cl-ionen resulteert in de vorming van natriumchloride (NaCl), een neutrale verbinding.
Samengevat: Natrium vormt een ionische binding met chloor door zijn valentie-elektron aan chloor te doneren, wat resulteert in de vorming van stabiele ionen die elkaar aantrekken vanwege hun tegengestelde ladingen. Deze aantrekking leidt tot de vorming van natriumchloride (NaCl).
 Wat veroorzaakt een toename van de snelheid van een chemische reactie tussen 2 vloeistoffen?
Wat veroorzaakt een toename van de snelheid van een chemische reactie tussen 2 vloeistoffen?  Onderzoekers ontdekken structuur van anti-verouderingshormoon
Onderzoekers ontdekken structuur van anti-verouderingshormoon Welke elementen zouden de grootste aantrekkingskracht voor elektronen hebben. Boron of zuurstofzwavel?
Welke elementen zouden de grootste aantrekkingskracht voor elektronen hebben. Boron of zuurstofzwavel?  Wat waren de 4 delen van John Atomic Theory?
Wat waren de 4 delen van John Atomic Theory?  Welke moleculen worden gesynthetiseerd in lichte reactie?
Welke moleculen worden gesynthetiseerd in lichte reactie?
 Amerikaanse burgemeesters omzeilen Trump om klimaatdoelen van Parijs te steunen
Amerikaanse burgemeesters omzeilen Trump om klimaatdoelen van Parijs te steunen Stijging van het zuurstofgehalte houdt verband met een oude explosie van leven, onderzoekers vinden
Stijging van het zuurstofgehalte houdt verband met een oude explosie van leven, onderzoekers vinden Zuivering van afvalwater kan leiden tot disbalans tussen stikstof en fosfor
Zuivering van afvalwater kan leiden tot disbalans tussen stikstof en fosfor Hoe klimaatverandering subalpiene wilde bloemengemeenschappen kan hervormen
Hoe klimaatverandering subalpiene wilde bloemengemeenschappen kan hervormen  Methaanuitstoot uit reservoirs neemt toe
Methaanuitstoot uit reservoirs neemt toe
Hoofdlijnen
- Welke factoren zijn betrokken bij de vorming van nieuwe soorten?
- Waarom gebruikt de genetica dieren voor hun erfelijkheidsexperimenten en niet mensen?
- Wat zijn drie voorbeelden van organisme?
- Welk organel omringt het celmembraan en bevat erfelijk materiaal?
- Waar zijn spiervezels van gemaakt?
- Wat eet een prokaryote?
- Nieuwe detectietechnieken kunnen droogtetolerantie in oude gewassen detecteren en kunnen nieuwe fokprogramma's informeren
- Hoe verandert osmose de vorm van een cel?
- Welke vormt nieuwe soorten?
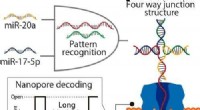
- Nanopore-technologie met DNA-computing detecteert gemakkelijk microRNA-patronen van longkanker
- 'S Werelds meest efficiënte productie van succinaat uit koolstofdioxide
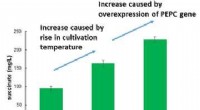
- Hoe temperatuur de carbonatatie in dranken beïnvloedt

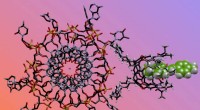
- Chemische neus snuffelt kritische verschillen in DNA-structuren
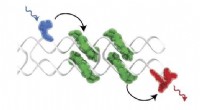
- Leren van fotosynthese:synthetische circuits kunnen lichtenergie oogsten
 Hoe wordt de wetenschap in je dagelijks leven gebruikt?
Hoe wordt de wetenschap in je dagelijks leven gebruikt?  Leg uit wat er gebeurt als zonlicht een chlorofylmolecuul raakt?
Leg uit wat er gebeurt als zonlicht een chlorofylmolecuul raakt?  Waarom is er heel weinig Astomphere de maan?
Waarom is er heel weinig Astomphere de maan?  Hoe zijn wetenschappelijk feit en een anders wet?
Hoe zijn wetenschappelijk feit en een anders wet?  Wat zijn enkele bronnen in de regio Great Plains?
Wat zijn enkele bronnen in de regio Great Plains?  Hoe microscopische machines in een oogwenk kapot kunnen gaan
Hoe microscopische machines in een oogwenk kapot kunnen gaan  Wat is het centrum van het massa van de aarde-maansysteem?
Wat is het centrum van het massa van de aarde-maansysteem?  Creatie van het meest perfecte grafeen
Creatie van het meest perfecte grafeen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

