
Wetenschap
Natrium-chloorbinding:bepaling van ionenladingen na elektronenoverdracht
Laten we dit opsplitsen:
* Natrium (Na) heeft één elektron in zijn buitenste schil. Het wil dit elektron kwijtraken om een stabiele elektronenconfiguratie te bereiken.
* Chloor (Cl) heeft zeven elektronen in de buitenste schil. Het wil één elektron winnen om een stabiele elektronenconfiguratie te bereiken.
Wanneer natrium en chloor binden:
* Natrium doneert het is één elektron met chloor.
* Natrium, dat een elektron heeft verloren, wordt een positief geladen ion (Na+).
* Chloor, dat een elektron heeft gewonnen, wordt een negatief geladen ion (Cl-).
Daarom heeft chloor, na acceptatie van het elektron, een negatieve lading (-1).
 Zijn verbindingen gemaakt door fysieke veranderingen?
Zijn verbindingen gemaakt door fysieke veranderingen?  Hoeveel moleculen ammoniak zitten er in 10 mol NH3?
Hoeveel moleculen ammoniak zitten er in 10 mol NH3?  Doteringsvrij, vochtstabiele organische lagen geven perovskiet-zonnecellen 21% efficiëntie
Doteringsvrij, vochtstabiele organische lagen geven perovskiet-zonnecellen 21% efficiëntie Overgebleven graan van brouwerijen kan worden omgezet in brandstof voor huizen
Overgebleven graan van brouwerijen kan worden omgezet in brandstof voor huizen Wat zijn enkele van het gebruik van zoutzuur?
Wat zijn enkele van het gebruik van zoutzuur?
 DeepShake gebruikt machine learning om de intensiteit van aardbevingen snel te schatten
DeepShake gebruikt machine learning om de intensiteit van aardbevingen snel te schatten Hoe Landforms Affect Weather
Hoe Landforms Affect Weather De puzzel om de ergste aardgaslozing in de geschiedenis te stoppen
De puzzel om de ergste aardgaslozing in de geschiedenis te stoppen Wat omhult de aarde?
Wat omhult de aarde?  Natuurspektakel:een Denali-gletsjer snelt bergafwaarts, mogelijke hinder voor klimmers en vergroot overstromingsrisico
Natuurspektakel:een Denali-gletsjer snelt bergafwaarts, mogelijke hinder voor klimmers en vergroot overstromingsrisico
Hoofdlijnen
- Waarom is het celmembraan van een plant belangrijk?
- Science Fair Project Ideas for Dentistry
- Welk deel van een plant is niet verteerbaar door mensen?
- 'Veggie'-dinosaurussen verschilden in de manier waarop ze hun voedsel aten
- Reproduceren alle levende wezens zich aseksueel?
- Welke structuur maakt bloedcellen en zorgen voor spieren om te hechten?
- Wat was het eerste organisme en hoe overleefde het vroege omstandigheden?
- Welk orgaan produceert enzymenhormonen en een alkalische vloeistof?
- Moleculaire modellen versus andere modellen:belangrijkste verschillen verklaard
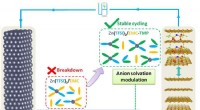
- Solvation-herschikking brengt stabiele zink/grafietbatterijen dichter bij commerciële netopslag
- Nieuwe techniek kan helpen bij het ontwerpen van vervuild waterfilter, menselijke weefsels

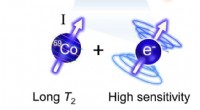
- Chemici ontwerpen chemische sonde voor het detecteren van minieme temperatuurverschuivingen in het lichaam
- Kleurveranderingstest om kankeronderzoek vooruit te helpen
- Het blootleggen van bacteriële celwandgeheimen om antibioticaresistentie te bestrijden

 Waarom sterft het organisme als ze voldoende water hebben?
Waarom sterft het organisme als ze voldoende water hebben?  Waar is levende materie meestal van gemaakt?
Waar is levende materie meestal van gemaakt?  Internettoegang via mobiele telefoons begint voor alle Cubanen
Internettoegang via mobiele telefoons begint voor alle Cubanen Wat is het effect van prokaryote indringers?
Wat is het effect van prokaryote indringers?  Schrijf een netto ionische vergelijking voor de reactie tussen hydrobromzuur en kaliumhydroxide?
Schrijf een netto ionische vergelijking voor de reactie tussen hydrobromzuur en kaliumhydroxide?  De atomaire dynamiek van zeldzame eeuwige elektrische velden
De atomaire dynamiek van zeldzame eeuwige elektrische velden Kwantumgeometrie biedt nieuwe inzichten in slimme materialen met schakelbare elektrische polariteit
Kwantumgeometrie biedt nieuwe inzichten in slimme materialen met schakelbare elektrische polariteit  Wat is het principe waarop een raket werkt?
Wat is het principe waarop een raket werkt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

