
Wetenschap
Reactie-evenwicht begrijpen:systemen met voorkeur voor producten
* Evenwicht betekent dat de snelheden van de voorwaartse en achterwaartse reacties gelijk zijn. Dit betekent niet dat er gelijke hoeveelheden reactanten en producten zijn, het betekent alleen dat de netto verandering in hun concentraties nul is.
* Evenwichtsconstante (K) is een maat voor de relatieve hoeveelheden reactanten en producten in evenwicht. Een hoge K-waarde geeft aan dat de reactie de vorming van producten bevordert.
* Voorkeur voor producten betekent dat de reactie in grotere mate in voorwaartse richting zal verlopen om producten te vormen, wat resulteert in een hogere concentratie van producten bij evenwicht.
Hier zijn enkele implicaties van een reactiesysteem in evenwicht met voornamelijk product:
* De verandering in de vrije energie van Gibbs (ΔG) is negatief , wat wijst op een spontane reactie.
* Het reactiequotiënt (Q) is groter dan de evenwichtsconstante (K) , wat betekent dat het systeem niet in evenwicht is en naar links zal verschuiven (in de richting van reactanten) om evenwicht te bereiken.
Samengevat , is een reactiesysteem in evenwicht met voornamelijk product een zeer gunstige reactie dat in belangrijke mate producten heeft gevormd.
 Waarom is argon zeer stabiel en niet reactief?
Waarom is argon zeer stabiel en niet reactief?  Wat doet waterstofgas?
Wat doet waterstofgas?  Wetenschappers vinden nieuwe manier om chirale moleculen te produceren die veiligere en goedkopere medicijnen kunnen opleveren
Wetenschappers vinden nieuwe manier om chirale moleculen te produceren die veiligere en goedkopere medicijnen kunnen opleveren Wat is de opgeloste stof en het oplosmiddel in benzine?
Wat is de opgeloste stof en het oplosmiddel in benzine?  Welke particalen in een atoom zijn de neucleus?
Welke particalen in een atoom zijn de neucleus?
Hoofdlijnen
- Welk enzym bouwt mRNA -moleculen op de code in DNA?
- Wat zijn de 6 elementen die het belangrijkst zijn in de biologie?
- Sekscelmutatie bevat veranderd DNA in welke cellen van het lichaam?
- Wat was het eerste organisme met een wervel?
- Waar wordt glucose gecreëerd?
- Welke functie van het reproductieve systeem is uitsluitend een vrouwelijk systeem?
- Microbiële structuren in het Antarctische meer zouden meer kunnen onthullen over hoe het leven zich ontwikkelde
- Voordelige lentetruffels of voortreffelijke Piemontese truffels? Nieuwe analysemethode kan voedselfraude opsporen
- Het organisme dat het doden is, is het?
- Meer zonne-energie dankzij titanium

- Machine learning biedt een nieuwe manier om chirale kristallen te ontwerpen

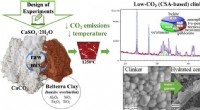
- Alternatief cement met lage ecologische voetafdruk ontwikkeld
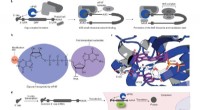
- Biochemici gebruiken nieuwe tool om mRNA te controleren door middel van licht
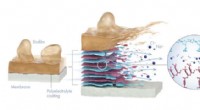
- Peel-off coating houdt ontzilting schoner en groener
 Team ontwikkelt productieproces voor biobrandstof in samenwerking met Noord-Amerikaanse onderzoekers
Team ontwikkelt productieproces voor biobrandstof in samenwerking met Noord-Amerikaanse onderzoekers Langetermijnstudie van gelijmde stalen wapeningen op een betonnen balk gaat 50e jaar in
Langetermijnstudie van gelijmde stalen wapeningen op een betonnen balk gaat 50e jaar in Wat is een minerale sluier?
Wat is een minerale sluier?  Wanneer een snelheid wordt teruggebracht tot de helft, hoe is de kinetische energie beïnvloed?
Wanneer een snelheid wordt teruggebracht tot de helft, hoe is de kinetische energie beïnvloed?  Wat is een van de gevonden DNA?
Wat is een van de gevonden DNA?  Laatste ijsgebied in de Noordelijke IJszee overleeft de eeuw misschien niet
Laatste ijsgebied in de Noordelijke IJszee overleeft de eeuw misschien niet Welk membraaneiwit is verantwoordelijk voor het verbinden van cellen met elkaar?
Welk membraaneiwit is verantwoordelijk voor het verbinden van cellen met elkaar?  Zijn kankersoorten nieuw ontwikkelde soorten?
Zijn kankersoorten nieuw ontwikkelde soorten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

