
Wetenschap
Hoe ziet een foto of watermolecuul eruit?
vereenvoudigde foto
* Vorm: Water (H₂o) is een gebogen molecuul, wat betekent dat het een V-achtige vorm heeft.
* atomen: Het heeft twee waterstofatomen (H) verbonden met een enkel zuurstofatoom (O).
* bindingen: De waterstofatomen zijn bevestigd aan het zuurstofatoom door covalente bindingen, die sterke bindingen zijn waar atomen elektronen delen.
Visuele weergave
U kunt vaak representaties van het watermolecuul vinden:
* Ball-and-Stick Model: Dit toont de atomen als bollen en de bindingen als sticks.
* Model voor ruimtevullen: Dit toont het molecuul met overlappende bollen, die de geschatte vorm van de elektronenwolk van het molecuul toont.
Wat maakt water uniek
* polariteit: Het zuurstofatoom is meer elektronegatief (trekt elektronen sterker aan) dan de waterstofatomen. Dit creëert een lichte negatieve lading in de buurt van de zuurstof en een lichte positieve lading nabij de hydrogenen, waardoor water een polair molecuul is.
* waterstofbinding: De polariteit van watermoleculen stelt hen in staat waterstofbruggen met elkaar te vormen, die zwak maar talrijk zijn, waardoor water zijn speciale eigenschappen krijgt, zoals zijn hoge kookpunt, oppervlaktespanning en het vermogen om veel stoffen op te lossen.
Denk er op deze manier aan:
Stel je een klein V-vormig molecuul voor met een iets negatief uiteinde en een enigszins positief uiteinde. Deze eenvoudige vorm, samen met zijn polariteit, is wat water zo belangrijk maakt voor het leven en geeft het al die unieke eigenschappen.
 Kovats berekenen Index
Kovats berekenen Index Natuurkundigen gebruiken wiskundige algoritmen om experimentele 3D-structuren van chromosomen te onderzoeken
Natuurkundigen gebruiken wiskundige algoritmen om experimentele 3D-structuren van chromosomen te onderzoeken Over het algemeen kan een polair oplosmiddel geen opgeloste stof oplossen?
Over het algemeen kan een polair oplosmiddel geen opgeloste stof oplossen?  Is vaseline een samengesteld woord?
Is vaseline een samengesteld woord?  Continue en stabiele laserwerking dankzij goedkope perovskieten bij kamertemperatuur
Continue en stabiele laserwerking dankzij goedkope perovskieten bij kamertemperatuur
 Verschillen tussen schaaldieren en insecten
Verschillen tussen schaaldieren en insecten  Natuurlijke veranderingen die een ecosysteem kunnen beïnvloeden
Natuurlijke veranderingen die een ecosysteem kunnen beïnvloeden  Hoe slaan planten overtollige suiker op?
Hoe slaan planten overtollige suiker op?  Grote hoeveelheden waardevolle energie, voedingsstoffen, water verloren in snel stijgende afvalwaterstromen ter wereld
Grote hoeveelheden waardevolle energie, voedingsstoffen, water verloren in snel stijgende afvalwaterstromen ter wereld Soorten planten in de Indische Oceaan
Soorten planten in de Indische Oceaan
Hoofdlijnen
- Wat creëren de ribosomen?
- Tijdens fotosynthese produceren planten suiker en wat?
- Wat is evolutionaire afweging?
- Wat is het doel van DNA -sequencing?
- Waarom leven sommige microben in je darmen en andere niet?
- Onderzoek naar fotosynthetische antennecomplexen maakt duidelijk hoe ze licht oogsten in planten, algen en bacteriën
- Kunnen mensen nog ouder worden? We hebben het maximale nog niet bereikt, zeggen sommige wetenschappers
- Wanneer heeft Schwann veel verschillende dierencellen waargenomen en tot een conclusie gekomen?
- Wat zijn enkele wetenschappelijke carrières?
- Gigantische moleculen in de vorm van Kandinsky-cirkels zijn giftig voor MRSA-bacteriën

- Ontdekking binnen het celcyclusproces om inzicht te krijgen in cellulaire ziekten
- Het licht zien:onderzoekers bieden oplossing voor efficiëntieprobleem van kunstmatige fotosynthese
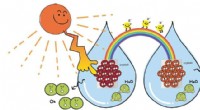
- Een beetje scheikunde uit de geschiedenis wissen

- Meteorietinslagen kunnen een onverwachte vorm van silica veroorzaken
 Wat is het niet goede materiaal bij het uitvoeren van thermische energie?
Wat is het niet goede materiaal bij het uitvoeren van thermische energie?  Waar is de Suns Energy opgeslagen in het proces van fotosynthese?
Waar is de Suns Energy opgeslagen in het proces van fotosynthese?  Welke energieconversie vindt plaats in een verzendende en ontvangende antenne?
Welke energieconversie vindt plaats in een verzendende en ontvangende antenne?  Het verwarde web van online televisie ontrafelen
Het verwarde web van online televisie ontrafelen Wat zijn de namen van de belangrijkste lithosperische platen?
Wat zijn de namen van de belangrijkste lithosperische platen?  Automatisch gendervooroordelen in films kwantificeren via beeldanalyse
Automatisch gendervooroordelen in films kwantificeren via beeldanalyse Hoe elektriciteit uw huis bereikt?
Hoe elektriciteit uw huis bereikt?  Wanneer een bal naar beneden rolt een hellingshelling, is de versnelling?
Wanneer een bal naar beneden rolt een hellingshelling, is de versnelling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

