
Wetenschap
Wat is elektrofiele toevoegingsreactie?
Elektrofiele toevoegingsreacties:een uitsplitsing
Een elektrofiele toevoegingsreactie is een type chemische reactie waarbij een elektrofiel (een elektronenminnende soort) bijdraagt aan een onverzadigd molecuul, zoals een alkeen of alkyn, wat resulteert in een verzadigd product.
Hier is een uitsplitsing van de belangrijkste componenten:
1. De elektrofiel:
* Een elektrofiel is een soort die wordt aangetrokken tot elektronenrijke gebieden. Het heeft meestal een positieve lading of een gedeeltelijk positieve lading.
* Gemeenschappelijke voorbeelden zijn:
* H+ (proton): Gevonden in sterke zuren zoals HCl, HBR, HI
* x+ (halogenen): Zoals br+, cl+, i+
* h2o: Hoewel neutraal, kan het werken als een elektrofiel vanwege de gedeeltelijke positieve lading op de waterstofatomen.
2. Het onverzadigde molecuul:
* Het molecuul dat een dubbele of drievoudige binding bevat (respectievelijk alkeen of alkyne) heeft een gebied met een hoge elektronendichtheid als gevolg van de PI -elektronen.
* Deze PI -elektronen worden gemakkelijk aangevallen door elektrofielen.
3. De toevoegingsstap:
* De elektrofiel valt de elektronenrijke PI-binding aan, verbreekt de dubbele of drievoudige binding en vormt een nieuwe enkele binding.
* Dit resulteert in de vorming van een carbocatie -tussenproduct, een positief geladen koolstofatoom.
* De carbocatie is zeer reactief en wordt meestal aangevallen door een nucleofiel (een elektronenrijke soort), wat leidt tot de vorming van het eindproduct.
4. Het product:
* Het product van een elektrofiele toevoegingsreactie is een verzadigd molecuul met een nieuwe enkele binding gevormd tussen de elektrofiel en het onverzadigde molecuul.
Voorbeeld:toevoeging van HBR aan Ethene
1. elektrofiel: H+ (proton) van HBr
2. Onverzadigd molecuul: Eteen (CH2 =CH2)
3. toevoeging: De H+ valt de PI -binding aan en vormt een carbocatie -tussenproduct.
4. nucleofiel: De br-anion valt de carbocatie aan en vormt het eindproduct, bromoethaan (CH3CH2BR).
Sleutelpunten:
* Het reactiemechanisme is over het algemeen een tweestapsproces:elektrofiele aanval gevolgd door nucleofiele aanval.
* De regiochemie (de positie van de elektrofiele en nucleofiele toevoeging) wordt bepaald door de regel van Markovnikov , die stelt dat de elektrofiel bijdraagt aan de koolstof met de meeste hydrogenen.
* Elektrofiele toevoegingsreacties zijn zeer belangrijk in de organische chemie en spelen een sleutelrol bij de synthese van verschillende verbindingen.
Toepassingen:
* Industriële processen: Productie van polymeren zoals polyethyleen en PVC.
* Laboratoriumsynthese: Synthese van verschillende organische moleculen, zoals haloalkanen, alcoholen en ethers.
* Biologische processen: Betrokken bij metabole routes zoals de synthese van vetzuren.
Inzicht in elektrofiele toevoegingsreacties is essentieel voor het begrijpen van veel organische chemische reacties en processen.
 Satellietweergave van post-tropische cycloon Jose die aan het vervagen is
Satellietweergave van post-tropische cycloon Jose die aan het vervagen is Welk levend ding op aarde is het meest voorkomen?
Welk levend ding op aarde is het meest voorkomen?  De VS verliest steeds sneller wetlands – hoe de particuliere sector kan helpen deze waardevolle hulpbronnen te beschermen
De VS verliest steeds sneller wetlands – hoe de particuliere sector kan helpen deze waardevolle hulpbronnen te beschermen  Klimaatverandering maakt Atlantische orkanen al heviger, studie vondsten
Klimaatverandering maakt Atlantische orkanen al heviger, studie vondsten Spanje getroffen door meer bosbranden terwijl hittegolf voortduurt
Spanje getroffen door meer bosbranden terwijl hittegolf voortduurt
Hoofdlijnen
- Wat worden cellen zonder kern of complexe organellen genoemd?
- Wat is het bijvoeglijk naamwoord voor genen?
- Hoe regelt uw lichaam de pH?
- Het choroïde en de oorschelp zijn vergelijkbaar omdat?
- Wat is een primitieve cel?
- Welke evolutie van embryologie?
- Wat is een bacterieel geslacht met wasachtig mycolzuur in de celwanden?
- Herdersactiviteiten overdag hebben geen negatieve invloed op gevlekte hyena's in Tanzania
- Heeft groot organisme meer chromosoom?
- Nieuwe techniek geeft polyurethaanafval een tweede leven

- Zelfherstellende batterijen:ingenieurs ontwikkelen een manier om batterijen met een hoge capaciteit en een lange levensduur te maken

- Hoe een interesse in geneesmiddelen voor bipolaire stoornis leidde tot een beter begrip van leukemie
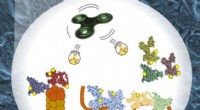
- Verder gaan dan de moleculen van Moeder Natuur om zich op radioactieve metalen te richten
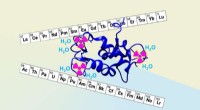
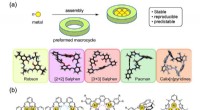
- Metaalcomplexen gemaakt van cyclische moleculen
 Bestaan alle levende wezens uit organische moleculen?
Bestaan alle levende wezens uit organische moleculen?  Insectenfrass wordt voedsel voor eiwitrijke microalgen
Insectenfrass wordt voedsel voor eiwitrijke microalgen  Hoe wordt verspreiding van gassen in water essentieel uitgelegd met voorbeeld?
Hoe wordt verspreiding van gassen in water essentieel uitgelegd met voorbeeld?  Hoeveel ionenparen arseen -elektronen in ASI3?
Hoeveel ionenparen arseen -elektronen in ASI3?  Zonder goed beheer raakt de Braziliaanse Cerrado misvormd en minder veerkrachtig tegen de klimaatverandering
Zonder goed beheer raakt de Braziliaanse Cerrado misvormd en minder veerkrachtig tegen de klimaatverandering  Barometrische druk en sneeuwstormen
Barometrische druk en sneeuwstormen  Kleine asteroïde ontdekt zaterdag valt uiteen boven Afrika
Kleine asteroïde ontdekt zaterdag valt uiteen boven Afrika Wat is de temperatuur van constellatie?
Wat is de temperatuur van constellatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

