
Wetenschap
Welke moleculen absorberen licht?
1. Moleculen met chromoforen:
* chromoforen zijn specifieke groepen atomen in een molecuul die verantwoordelijk zijn voor het absorberen van licht. Ze bevatten meestal geconjugeerde systemen van afwisselende enkele en dubbele bindingen, die delocalisatie van elektronen mogelijk maken.
* Voorbeelden:
* Organische kleurstoffen: Veel organische kleurstoffen zoals indigo, alizarine en chlorofyl bevatten chromoforen die zichtbaar licht absorberen, waardoor ze hun levendige kleuren krijgen.
* eiwitten: Eiwitten kunnen chromoforen zoals heem in hemoglobine hebben, die licht absorberen in het zichtbare spectrum en bloed zijn rode kleur geeft.
* pigmenten: Pigmenten die in kunst worden gebruikt, zoals cadmiumgeel en ftalocyanineblauw, bevatten ook chromoforen die specifieke golflengten van licht absorberen.
2. Moleculen met specifieke functionele groepen:
* Bepaalde functionele groepen, zoals carbonyl (C =O) en Nitro (NO2), kunnen ook licht absorberen.
* Voorbeelden:
* ketonen en aldehyden: Deze moleculen bevatten carbonylgroepen die licht absorberen in het UV -gebied.
* nitroverbindingen: Deze verbindingen absorberen licht in het zichtbare gebied, wat leidt tot hun gele of oranje kleuren.
3. Moleculen met specifieke moleculaire structuren:
* De algehele vorm en opstelling van atomen in een molecuul kan ook de lichtabsorptie -eigenschappen beïnvloeden.
* Voorbeelden:
* cyclische moleculen: Bepaalde cyclische moleculen, zoals benzeen, absorberen licht in het UV -gebied vanwege hun aromatische structuur.
* stereochemie: De ruimtelijke opstelling van atomen in een molecuul (stereochemie) kan ook de lichtabsorptie beïnvloeden, omdat verschillende stereoisomeren verschillende absorptie -eigenschappen kunnen hebben.
4. Moleculen met specifieke elektronische overgangen:
* Wanneer een molecuul licht absorbeert, bevordert het een elektron tot een hoger energieniveau. Het type elektronische overgang (bijv. Sigma naar sigma*, pi tot pi*, n tot pi*) dat optreedt, bepaalt de golflengte van geabsorbeerde licht.
* Voorbeelden:
* UV-vis spectroscopie: Deze techniek wordt gebruikt om de elektronische overgangen van moleculen te bestuderen en hun absorptie -eigenschappen te bepalen in de UV- en zichtbare gebieden van het elektromagnetische spectrum.
Samenvattend kunnen veel soorten moleculen licht absorberen, afhankelijk van hun:
* Aanwezigheid van chromoforen
* Functionele groepen
* Moleculaire structuur
* Elektronische overgangen
De specifieke golflengten die worden geabsorbeerd door een molecuul worden bepaald door de unieke combinatie van deze factoren. Dit is de reden waarom verschillende moleculen verschillende kleuren hebben, verschillende golflengten van licht absorberen en worden gebruikt voor verschillende toepassingen, waaronder kleurstoffen, pigmenten en spectroscopie.
 Als PH 7,5 is, wat is dan de waarde van H?
Als PH 7,5 is, wat is dan de waarde van H?  Nieuwe macrolacton-database kan helpen bij het ontdekken van medicijnen, Onderzoek
Nieuwe macrolacton-database kan helpen bij het ontdekken van medicijnen, Onderzoek Waarom hebben ionen een positieve of negatieve lading?
Waarom hebben ionen een positieve of negatieve lading?  Wat zijn de voordelen van dampstoomreinigers ten opzichte van chemische reinigers?
Wat zijn de voordelen van dampstoomreinigers ten opzichte van chemische reinigers?  Welk zout wordt gemaakt wanneer natriumhydroxide reageert met zuur?
Welk zout wordt gemaakt wanneer natriumhydroxide reageert met zuur?
 Wat gebeurt er als het magnetische noorden en het ware noorden op één lijn liggen?
Wat gebeurt er als het magnetische noorden en het ware noorden op één lijn liggen? Zijn er andere natuurbeschermingswetten die in het leven lijken te verschijnen?
Zijn er andere natuurbeschermingswetten die in het leven lijken te verschijnen?  Hoe worden grondstoffen in de natuur gevonden?
Hoe worden grondstoffen in de natuur gevonden?  Onderzoek:effectiviteit van programma dat boeren betaalt om water te besparen
Onderzoek:effectiviteit van programma dat boeren betaalt om water te besparen Zijn mist en mist hetzelfde?
Zijn mist en mist hetzelfde?
Hoofdlijnen
- Welke van de volgende paden produceert de meeste NADH en de minste ATP?
- Wat is de specifieke celontvanger bekend?
- Wat doet ethanol in een DNA-extractie?
- Wat zijn drie verschil tussen virussen en bacteriën?
- Wat is een term die de manipulatie van DNA in cellen beschrijft om ziektebestendige gewassen en dieren voor landbouw te produceren?
- Wat is een groot verschil in de extracellulaire matrix -ECM tussen planten- en dierlijke cellen?
- Is het mogelijk om bacteriekweekbuizen te hergebruiken?
- In welke tak van de geneeskunde is gespecialiseerd in het onderzoek van het musculoskeletale systeem?
- Blueprint laat zien hoe planten een suikertransportbaan aanleggen
- Techniek om functionele materialen te maken op basis van polymeren van metaalclusters
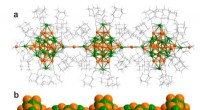
- Een stap in de richting van metaal-organische raamwerksynthese
- Panel kondigt Nobelprijs voor scheikunde 2020 aan

- Nieuwe genetische methode verbetert de efficiëntie van het enzym

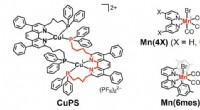
- Grote stappen voor het vastleggen van koolstof met behulp van aarde-overvloedige elementen als fotokatalytisch systeem
 Hoe snel is Mach 1.2 in MPH?
Hoe snel is Mach 1.2 in MPH?  Samsung-onderzoekers:efficiëntere quantum dots zonder zware metalen
Samsung-onderzoekers:efficiëntere quantum dots zonder zware metalen Een heldere ster kan er dimmer uitzien dan een minder als de is?
Een heldere ster kan er dimmer uitzien dan een minder als de is?  Waarom houden wetenschappers gedetailleerde gegevens en procedures bij?
Waarom houden wetenschappers gedetailleerde gegevens en procedures bij?  Welke hernieuwbare energiebronnen hebben van de zon nodig?
Welke hernieuwbare energiebronnen hebben van de zon nodig?  Wat zijn de overeenkomsten van hellende vlakken en wiggen?
Wat zijn de overeenkomsten van hellende vlakken en wiggen?  Waarom zou een kamer klaar zijn nadat het huis was gebouwd die wordt verwarmd door een aardgasoven met geforceerde lucht, maar geen warmte?
Waarom zou een kamer klaar zijn nadat het huis was gebouwd die wordt verwarmd door een aardgasoven met geforceerde lucht, maar geen warmte?  Wat is ader in de geologie?
Wat is ader in de geologie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

