
Wetenschap
De aantrekkingskracht tussen watermoleculen is het resultaat van water?
Dit is waarom:
* polariteit: Watermoleculen zijn polair, wat betekent dat ze een enigszins positief uiteinde hebben (nabij de waterstofatomen) en een enigszins negatief uiteinde (nabij het zuurstofatoom).
* Waterstofbindingen: Het enigszins positieve waterstofuiteinde van het ene watermolecuul wordt aangetrokken door het enigszins negatieve zuurstofuiteinde van een ander watermolecuul. Deze aantrekkingskracht wordt een waterstofbinding genoemd.
Waterstofbindingen zijn relatief zwak in vergelijking met covalente bindingen, maar ze zijn sterk genoeg om watermoleculen bij elkaar te houden, waardoor water veel van zijn unieke eigenschappen krijgt:
* Hoog kookpunt: Water heeft een hoger kookpunt dan veel andere vloeistoffen omdat waterstofbruggen moeten worden verbroken om van water te veranderen van een vloeistof naar een gas.
* Hoge oppervlaktespanning: Waterstofbindingen creëren een sterke samenhangende kracht tussen watermoleculen, waardoor water een hoge oppervlaktespanning krijgt.
* Uitstekend oplosmiddel: De polariteit van watermoleculen stelt hen in staat om veel stoffen op te lossen.
Dus de aantrekkingskracht tussen watermoleculen is een gevolg van de polaire aard van de moleculen en de vorming van waterstofbruggen .
 Studie onderzoekt hoe schone lucht de gemeentelijke obligatiemarkt beïnvloedt
Studie onderzoekt hoe schone lucht de gemeentelijke obligatiemarkt beïnvloedt  Hoe methaangas te comprimeren tot vloeibaar
Hoe methaangas te comprimeren tot vloeibaar  Wat is moeilijker - natuurkunde of chemie?
Wat is moeilijker - natuurkunde of chemie?  Welke massa vaste AGCL wordt verkregen wanneer 25 ml 0,068 m Agno3 reageert met overtollige waterige HCl?
Welke massa vaste AGCL wordt verkregen wanneer 25 ml 0,068 m Agno3 reageert met overtollige waterige HCl?  Wat is een chemische verbindingen bestaande uit dezelfde elementen?
Wat is een chemische verbindingen bestaande uit dezelfde elementen?
 De therapeutische kracht van water aanboren om de gezondheidskosten te verlagen
De therapeutische kracht van water aanboren om de gezondheidskosten te verlagen Subductie van de Pacifische plaat resulteerde in de vernietiging van het Noord-Chinese Craton
Subductie van de Pacifische plaat resulteerde in de vernietiging van het Noord-Chinese Craton Beschrijf wat een korstmos is en waar je het in de hoogste overvloed zou vinden?
Beschrijf wat een korstmos is en waar je het in de hoogste overvloed zou vinden?  Wat wordt bedoeld met de intensiteit van het elektrische veld?
Wat wordt bedoeld met de intensiteit van het elektrische veld?  Kunststofvolgend jacht voegt een vleugje milieubewustzijn toe aan oceaanraces
Kunststofvolgend jacht voegt een vleugje milieubewustzijn toe aan oceaanraces
Hoofdlijnen
- Wat is de centrale dogma -biologie?
- Wat wordt er in alleen plantencellen gevonden die fotosynthese ondergaan?
- Dierlijke cellen slaan overtollige suiker op in de vorm van een polysacharide genaamd zetmeel?
- Als een eigenschap een organisme minder geneigd was om te overleven en te reproduceren wat zou er dan gebeuren, het allel voor eigenschap?
- Wat zijn 2 voorbeelden van levenswetenschap?
- Wat is cellulair cytoplasma voornamelijk samengesteld uit welke stof?
- Wat wordt de naam gegeven om delen van het menselijk lichaam en hun functies te bestuderen?
- Wat doodt de Argentijnse walvissen?
- Het orgaansysteem van het lichaam dat functioneert in de secretie van regulerende moleculen, hormonen genaamd, is systeem-?
- Nieuwe behandeling ontsluit potentieel voor het bakken van frambozen

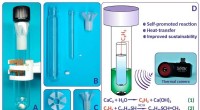
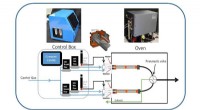
- Chemici vinden een efficiënte thermische camera uit om de kosten van chemisch onderzoek te verlagen
- Spoordampgenerator voor het opsporen van explosieven, verdovende middelen
- Wetenschappers maken waterfiltratiemembranen die zichzelf kunnen reinigen

- Chemici ontdekken hoe blauw licht blindheid versnelt

 Wie heeft de planeet Aarde genoemd?
Wie heeft de planeet Aarde genoemd?  Waar komt polycarbonaatplastic vandaan en waar is en waar is uitgevonden?
Waar komt polycarbonaatplastic vandaan en waar is en waar is uitgevonden?  Studie onderzoekt hoe media over de hele wereld nieuws over klimaatverandering framen
Studie onderzoekt hoe media over de hele wereld nieuws over klimaatverandering framen Wat produceert Proton Motive Force?
Wat produceert Proton Motive Force?  IJzer in het vuur:Onderzoekers bepalen hoe ijzerafzettingen ontstaan
IJzer in het vuur:Onderzoekers bepalen hoe ijzerafzettingen ontstaan  Gespecialiseerd onderdeel van een cel die een speciaal functie klein orgaan in cel uitvoert?
Gespecialiseerd onderdeel van een cel die een speciaal functie klein orgaan in cel uitvoert?  Ziekenhuizen verdedigen tegen levensbedreigende cyberaanvallen
Ziekenhuizen verdedigen tegen levensbedreigende cyberaanvallen Vertrouwen in algoritmisch advies van computers kan ons blind maken voor fouten, zegt onderzoek
Vertrouwen in algoritmisch advies van computers kan ons blind maken voor fouten, zegt onderzoek
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

