
Wetenschap
Hoe bepaal je of een monster van materie vaste vloeistof of gas is?
1. Vorm en volume
* vaste stoffen: Hebben een duidelijke vorm en een duidelijk volume. Ze behouden hun vorm en volume, zelfs wanneer ze naar een andere container worden verplaatst.
* vloeistoffen: Heb een duidelijk volume maar neem de vorm van hun container. Ze vullen de onderkant van een container, maar zullen niet noodzakelijkerwijs uitbreiden om de hele container te vullen.
* gassen: Hebben geen duidelijke vorm of volume. Ze zullen uitbreiden om de hele container te vullen waarin ze worden geplaatst.
2. Samperrukbaarheid
* vaste stoffen: Over het algemeen niet samendrukbaar. Hun moleculen zijn strak verpakt en worden weerstaan dichter bij elkaar te worden geperst.
* vloeistoffen: Enigszins samendrukbaar. Hun moleculen zijn dichter bij elkaar dan gasmoleculen, maar hebben nog steeds wat ruimte tussen hen.
* gassen: Zeer samendrukbaar. Hun moleculen zijn ver uit elkaar en kunnen dichter bij elkaar worden geperst.
3. Flow
* vaste stoffen: Niet stromen. Ze handhaven hun vorm en weerstaan vervorming.
* vloeistoffen: Stroom gemakkelijk. Ze nemen de vorm van hun container aan en kunnen worden gegoten.
* gassen: Stroom gemakkelijk. They expand to fill their container and can be easily compressed.
4. Andere eigenschappen
* Dichtheid: Vaste stoffen hebben over het algemeen hogere dichtheden dan vloeistoffen, die hogere dichtheden hebben dan gassen.
* Thermische uitbreiding: Vaste stoffen, vloeistoffen en gassen breiden allemaal uit wanneer ze worden verwarmd, maar gassen breiden het meest uit.
voorbeelden
* solide: Rots, ijs, hout
* vloeistof: Water, olie, kwik
* gas: Lucht, zuurstof, koolstofdioxide
Onthoud:
* De toestand van materie kan veranderen met temperatuur en druk. Water kan bijvoorbeeld bestaan als een vaste stof (ijs), een vloeistof (water) of een gas (stoom).
* Er zijn enkele uitzonderingen op deze algemene regels, maar ze bieden een goed startpunt voor het begrijpen van de verschillen tussen vaste stoffen, vloeistoffen en gassen.
 Welke soorten atomen geven nucleaire straling af?
Welke soorten atomen geven nucleaire straling af?  Wat zijn het gebruik van koolstofdioxidedioxide?
Wat zijn het gebruik van koolstofdioxidedioxide?  Waarom groene ammoniak dat misschien niet is
Waarom groene ammoniak dat misschien niet is  Wat gebeurt er met de concentratie hydroxide-ionen in water als een base wordt toegevoegd?
Wat gebeurt er met de concentratie hydroxide-ionen in water als een base wordt toegevoegd?  Wat gebeurt er als u een Iron III nitraat AQ -oplossing toevoegt aan koper?
Wat gebeurt er als u een Iron III nitraat AQ -oplossing toevoegt aan koper?
 Geneesmiddelen vormen een wereldwijd milieurisico, experts waarschuwen
Geneesmiddelen vormen een wereldwijd milieurisico, experts waarschuwen Moeten we afscheid nemen van de unieke natuur van de Noordpool?
Moeten we afscheid nemen van de unieke natuur van de Noordpool? Smog in Delhi bereikt noodniveaus tijdens bezoek van Britse prins Charles
Smog in Delhi bereikt noodniveaus tijdens bezoek van Britse prins Charles India's droogperiode van 50 jaar en daaropvolgende omkering - strijd tussen natuurlijke en antropogene variabiliteit
India's droogperiode van 50 jaar en daaropvolgende omkering - strijd tussen natuurlijke en antropogene variabiliteit Hoe maak je een Diorama van een Spider Habitat
Hoe maak je een Diorama van een Spider Habitat
Hoofdlijnen
- Wat zijn de drie belangrijkste koninkrijken van eukaryotisch?
- Hoe verschilt de DNA -prokaryote van in een eukaroyte?
- Ongevaarlijk of dodelijk? Onderzoek naar de evolutie van E. coli
- Wat wordt gebruikt om de genetische code van DNA -ribosomen te dragen?
- Wat is het doel van transport voor eiwitten?
- Waar groeit Candida -schimmels op?
- Hoe communiceren de lever en de nieren en welke hormonen worden gebruikt?
- Wat reptielenbotten ons kunnen leren over het gevaarlijke verleden van de aarde
- Wat gebruiken wetenschappers hulpmiddelen?
- Wetenschappers werpen licht op nieuw goedkoop materiaal om in het donker te zien

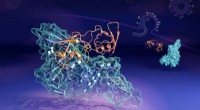
- Neutronen vangen vormveranderend coronavirus-eiwitcomplex op heterdaad
- Bergen afval kunnen leiden tot nieuwe productie in de VS, banen
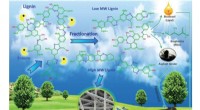
- De eerste ontdekking ter wereld kan de nieuwe groene ammoniakeconomie voeden

- Onderzoekers ontsluiten kankerverwekkend mechanisme van E. coli-toxine met synthetische biologie

 Leg uit waarom een voorwerp onder water lichter aanvoelt als het in de lucht is?
Leg uit waarom een voorwerp onder water lichter aanvoelt als het in de lucht is?  Voedseladvertenties op Twitch kunnen leiden tot trek, aankopen
Voedseladvertenties op Twitch kunnen leiden tot trek, aankopen Wat gebeurt er om afstand te doen als een eenvoudige machine helpt om de kracht te verminderen?
Wat gebeurt er om afstand te doen als een eenvoudige machine helpt om de kracht te verminderen?  De zon is erg groot in vergelijking met de maan?
De zon is erg groot in vergelijking met de maan?  De meeste dieren en planten hebben groepscellen met een vergelijkbare structuurfunctie die zijn georganiseerd?
De meeste dieren en planten hebben groepscellen met een vergelijkbare structuurfunctie die zijn georganiseerd?  Welke 3 vaste stoffen samentrekken bij koeling?
Welke 3 vaste stoffen samentrekken bij koeling?  Wat zijn de transformaties van energie die moeten gebeuren om geothermische electiciteit te veranderen?
Wat zijn de transformaties van energie die moeten gebeuren om geothermische electiciteit te veranderen?  Welke factoren helpen het type grond te bepalen, zoals diktelagen in hun samenstelling?
Welke factoren helpen het type grond te bepalen, zoals diktelagen in hun samenstelling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

