
Wetenschap
Wat definieert de tweede wet van de thermodynamica?
De entropie van een geïsoleerd systeem kan in de loop van de tijd nooit afnemen en het blijft alleen constant als alle processen omkeerbaar zijn.
Hier is een uitsplitsing van de sleutelconcepten:
* Entropie: Entropie is een maat voor wanorde of willekeur in een systeem. Hoe meer een systeem een systeem is, hoe hoger de entropie.
* geïsoleerd systeem: Een geïsoleerd systeem is een systeem dat geen energie uitruilt of materie met zijn omgeving.
* omkeerbaar proces: Een omkeerbaar proces is een proces dat kan worden teruggedraaid zonder enige spoor achter te laten op de omgeving.
in eenvoudiger termen:
* Warmte stroomt altijd van een heet object naar een koud object. Dit komt omdat het hete object een hogere entropie heeft en de warmtestroom helpt om de entropie tussen de twee objecten gelijk te maken.
* dingen vallen meestal uit elkaar. Naarmate de tijd verstrijkt, worden systemen natuurlijk meer ongeordend en minder georganiseerd. Dit is de reden waarom een rommelige kamer de neiging heeft rommelig te blijven, tenzij je actief werkt om het op te ruimen.
* U kunt geen eeuwige bewegingsmachine maken. Elke machine die probeert energie uit niets te creëren, zal uiteindelijk falen omdat het de tweede wet van de thermodynamica schendt.
Implicaties van de tweede wet:
* Het universum wordt constant meer wanordelijk. Dit is een fundamenteel principe van het universum en heeft diepgaande implicaties voor ons begrip van de kosmos.
* De tweede wet beperkt de efficiëntie van motoren en andere apparaten. Geen enkele motor kan 100% efficiënt zijn omdat sommige energie altijd verloren gaat als warmte.
* Het biedt een raamwerk voor het begrijpen van de richting van spontane verandering. De tweede wet helpt ons te begrijpen waarom bepaalde processen spontaan plaatsvinden, terwijl anderen dat niet doen.
Belangrijke opmerking: De tweede wet van de thermodynamica is alleen van toepassing op geïsoleerde systemen. In open systemen, zoals levende organismen of industriële processen, kan entropie lokaal afnemen, maar alleen ten koste van toenemende entropie in de omgeving.
 Wetenschappers krijgen vroeg inzicht in orkaanschade aan Caribische koraalriffen
Wetenschappers krijgen vroeg inzicht in orkaanschade aan Caribische koraalriffen Onderzoek naar afval op zee telt afval van Texas tot Florida
Onderzoek naar afval op zee telt afval van Texas tot Florida Darwin of Kimura? Natuurlijke selectie puur toeval? Nieuw literatuuronderzoek heeft tot doel een verhit debat te verhelderen
Darwin of Kimura? Natuurlijke selectie puur toeval? Nieuw literatuuronderzoek heeft tot doel een verhit debat te verhelderen  Het team ontdekt hoe de zoutste vijver ter wereld aan zijn zout komt
Het team ontdekt hoe de zoutste vijver ter wereld aan zijn zout komt  Oceaanhypoxie voor de kust van de Pacific Northwest verontrustender dan ooit
Oceaanhypoxie voor de kust van de Pacific Northwest verontrustender dan ooit
Hoofdlijnen
- Wat is een voorbeeld van mitochondria?
- Haaien evolueerden vliegtuigachtige attributen om in habitats te passen
- Onderzoekers tonen nieuwe techniek die DNA kan 'proeven'
- Nieuwe inzichten helpen verklaren waarom seksuele interacties tussen mensen van hetzelfde geslacht zo belangrijk zijn voor vrouwelijke bonobo's
- Waarom worden culturele en biologische controles op chemische stoffen geïntegreerd in programma's voor ongediertebestrijding?
- Hoe stuifmeel werkt
- Wat is een datawetenschapper?
- De COVID-wiebel opvangen:Onderzoekers ontwikkelen een nieuwe manier om te visualiseren hoe spike-eiwit zijn bewegingen laat zien
- Hoe je de biomassa van planten kunt stimuleren:Biologen ontdekken het moleculaire verband tussen de beschikbaarheid van voedingsstoffen en de groei
- Wolachtig materiaal kan zich herinneren en van vorm veranderen

- Machine learning stroomlijnt het zoeken naar efficiëntere chemische reacties drastisch
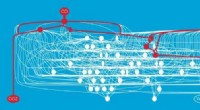
- Polarisatie van broommolecuul in vanadiumoxideclusterholte en nieuwe bromering van alkaan
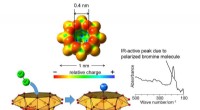
- Nieuwe methode voor het labelen van DNA-basen voor sequencing
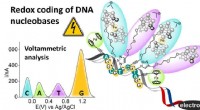
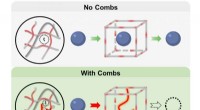
- Hydrogels met fijngetande moleculaire kammen kunnen duurzame implantaten voor glucosemonitoring maken
 In een experiment om te zien of het comfort van stoelen in een klaslokaal verschil maakt hoe lang studenten zullen werken aan wiskundeproblemen, was één groep standaard en opgevuld comforta?
In een experiment om te zien of het comfort van stoelen in een klaslokaal verschil maakt hoe lang studenten zullen werken aan wiskundeproblemen, was één groep standaard en opgevuld comforta?  De rauwe kracht van menselijke beweging
De rauwe kracht van menselijke beweging NASA meet potentiële tropische cycloon 10s temperatuur
NASA meet potentiële tropische cycloon 10s temperatuur Blockadia-kaart onthult wereldwijde schaal van antifossiele brandstofbeweging
Blockadia-kaart onthult wereldwijde schaal van antifossiele brandstofbeweging Wat gebeurt er als elektriciteit water raakt?
Wat gebeurt er als elektriciteit water raakt?  5 evidence-based manieren waarop docenten leerlingen met problemen kunnen helpen
5 evidence-based manieren waarop docenten leerlingen met problemen kunnen helpen In een chemische reactie is de totale massa reactanten 10,0 gram die de producten moeten zijn?
In een chemische reactie is de totale massa reactanten 10,0 gram die de producten moeten zijn?  Wat besteedt geen energie?
Wat besteedt geen energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

