
Wetenschap
Waarom is benzine minder dicht dan water?
* Water: Watermoleculen (h₂o) zijn polaire . Dit betekent dat ze een enigszins positief uiteinde en een enigszins negatief uiteinde hebben als gevolg van de opstelling van hun waterstof- en zuurstofatomen. Met deze polariteit kunnen watermoleculen sterke waterstofbindingen vormen met elkaar, het creëren van een strak gepakte structuur.
* benzine: Benzine is een mengsel van koolwaterstoffen, die nonpolar zijn . Deze moleculen bestaan uit voornamelijk koolstof- en waterstofatomen, die elektronen gelijkmatiger delen. Dit gebrek aan polariteit betekent dat koolwaterstofmoleculen zwakkere intermoleculaire krachten (voornamelijk van der Waals -krachten) hebben die ze bij elkaar houden.
Dichtheid en moleculaire krachten:
* Dichtheid is een maat voor hoeveel massa in een bepaald volume wordt verpakt.
* sterkere intermoleculaire krachten leiden tot een nauwere verpakking van moleculen, wat resulteert in een hogere dichtheid.
Samenvattend: De sterke waterstofbindingen van water creëren een dichtere structuur dan de zwakkere krachten tussen koolwaterstofmoleculen in benzine. Dit verschil in dichtheid is de reden waarom benzine op water zweeft.
 Waarom zou je aandacht besteden aan de fysieke toestanden van alle reactanten en producten bij het schrijven van evenwichtsconstante-uitdrukkingen?
Waarom zou je aandacht besteden aan de fysieke toestanden van alle reactanten en producten bij het schrijven van evenwichtsconstante-uitdrukkingen?  Kun je in chloor zitten terwijl je een chocoladereactie hebt?
Kun je in chloor zitten terwijl je een chocoladereactie hebt?  Sterke constructies realiseren met koolstofvezelversterkte kunststoffen
Sterke constructies realiseren met koolstofvezelversterkte kunststoffen Hoe verschillen de smelt- en kookpunten van water van die een suikerwateroplossing?
Hoe verschillen de smelt- en kookpunten van water van die een suikerwateroplossing?  Wat voor soort gas is in Irn Bru?
Wat voor soort gas is in Irn Bru?
 'Als ze maar betere levenskeuzes maakten.' Hoe simplistische verklaringen van armoede en voedselonzekerheid de plank misslaan
'Als ze maar betere levenskeuzes maakten.' Hoe simplistische verklaringen van armoede en voedselonzekerheid de plank misslaan  Hoeveel water is er op aarde?
Hoeveel water is er op aarde?  Studie signaleert nieuwe hoop voor Rockall olie- en gasexploratie
Studie signaleert nieuwe hoop voor Rockall olie- en gasexploratie Halve marathon Delhi gaat ondanks smog door rechtbank regels
Halve marathon Delhi gaat ondanks smog door rechtbank regels Wat is een kenmerken verwijst naar Savannah Biome maar niet gematigd Prairie Biome?
Wat is een kenmerken verwijst naar Savannah Biome maar niet gematigd Prairie Biome?
Hoofdlijnen
- Wat zijn de drie systemen waaruit vasculaire planten bestaat?
- Elementen van nucleïnezuren
- Hoe plantencellen het potentieel voor zelfbeschadiging neutraliseren
- Hoe samenwerking de concurrentie bij apen kan overtroeven
- Ontbreekt de plantencel een kern?
- Waar kwam DNA -informatie vandaan als er geen God is?
- Hoe DNA 'proofreader'-eiwitten hun leesmateriaal kiezen en bewerken
- Wat zijn drie redenen om DNA uit een menselijk onderwerp te extraheren?
- Wat is osmotische lyse?
- Wetenschappers creëren nanomaterialen die zich herconfigureren als reactie op biochemische signalen
- Laatste onbekende structuur van HIV-1 opgelost, weer een stap in de strijd tegen het aids-virus
- Metamaterialen bieden multifunctionele materialen voor engineering

- Levensechte scheikunde gemaakt in laboratoriumonderzoek naar manieren om de oorsprong van het leven te bestuderen
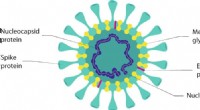
- Antivirale oppervlakken, oppervlaktecoatings en hun werkingsmechanismen
 Is lucht hetzelfde als Carbon Doixed?
Is lucht hetzelfde als Carbon Doixed?  Eerste bewijs van gigantische overblijfselen van sterexplosies
Eerste bewijs van gigantische overblijfselen van sterexplosies Wat is de laag grond die verweerde rotsen bevat?
Wat is de laag grond die verweerde rotsen bevat?  Wat is functionele dissociatie?
Wat is functionele dissociatie?  Caloriearm dieet:een langer leven?
Caloriearm dieet:een langer leven?  Verrassende vondst onthult nieuwe mogelijkheden voor halfgeleidermateriaal
Verrassende vondst onthult nieuwe mogelijkheden voor halfgeleidermateriaal Klimaatverandering zorgt voor snelle verschuivingen tussen hoge en lage waterstanden op de Grote Meren
Klimaatverandering zorgt voor snelle verschuivingen tussen hoge en lage waterstanden op de Grote Meren Autofabrikanten kiezen voor Trump in juridisch gevecht met Californië
Autofabrikanten kiezen voor Trump in juridisch gevecht met Californië
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

