
Wetenschap
Hoe identificeer je de relatieve massa -relaitieve lading en locatie van drie kleiner subatomair deeltje een atoom?
1. Protonen:
* Relatieve massa: 1 AMU (atomaire massa -eenheid)
* Relatieve lading: +1
* Locatie: In de kern van het atoom.
2. Neutronen:
* Relatieve massa: 1 AMU (ongeveer hetzelfde als protonen)
* Relatieve lading: 0 (neutraal)
* Locatie: In de kern van het atoom, naast protonen.
3. Elektronen:
* Relatieve massa: Verwaarloosbaar (ongeveer 1/1836 AMU in vergelijking met protonen en neutronen)
* Relatieve lading: -1
* Locatie: De kern ronddraaien in een wolk van waarschijnlijkheid die een elektronenwolk wordt genoemd. De specifieke energieniveaus en vormen van deze orbitalen worden gedefinieerd door kwantummechanica.
Sleutelpunten:
* Atomisch nummer: Het aantal protonen in de kern van een atoom bepaalt het atoomnummer en identificeert het element.
* Massienummer: De som van protonen en neutronen in de kern van een atoom bepaalt zijn massa -getal.
* isotopen: Atomen van hetzelfde element kunnen verschillende aantallen neutronen hebben, wat resulteert in isotopen. Isotopen hebben hetzelfde atoomnummer maar verschillende massagummers.
* neutraliteit: In een neutraal atoom is het aantal protonen (positieve lading) gelijk aan het aantal elektronen (negatieve lading). Dit resulteert in een netto lading van nul.
Hoe te onthouden:
* protonen: Zie ze als de "positieve" deeltjes in het "proton" -kern.
* neutronen: Zie ze als de "neutrale" deeltjes in de "neutronen" kern.
* elektronen: Beschouw ze als de "negatieve" deeltjes "elektron" icitisch in een baan om de kern.
Laat het me weten als je een van deze concepten verder wilt verkennen!
 Zinkmetaal reageert met zoutzuur volgens de volgende gebalanceerde vergelijking?
Zinkmetaal reageert met zoutzuur volgens de volgende gebalanceerde vergelijking?  Waarom buigen ionische verbindingen?
Waarom buigen ionische verbindingen?  Structurele en dynamische verschillen tussen selectieve en niet-selectieve ionkanalen
Structurele en dynamische verschillen tussen selectieve en niet-selectieve ionkanalen Wat gebeurt er met natrium als het zijn buitenste elektron verliest?
Wat gebeurt er met natrium als het zijn buitenste elektron verliest?  Als een stof faseverandering ondergaat, wat gebeurt er dan?
Als een stof faseverandering ondergaat, wat gebeurt er dan?
 Slachthuis Illinois grootste stikstofvervuiler van waterwegen in VS, studie vondsten
Slachthuis Illinois grootste stikstofvervuiler van waterwegen in VS, studie vondsten Amerikaans energiekolonialisme een belangrijke oorzaak van de orkaan Maria-crisis in Puerto Rico
Amerikaans energiekolonialisme een belangrijke oorzaak van de orkaan Maria-crisis in Puerto Rico Gletsjers verliezen 9 biljoen ton ijs in een halve eeuw
Gletsjers verliezen 9 biljoen ton ijs in een halve eeuw Wat is wetenschappelijke beweging?
Wat is wetenschappelijke beweging?  Noordpool binnenkort ijsvrij in zomer
Noordpool binnenkort ijsvrij in zomer
Hoofdlijnen
- Welke binding vormt zich tussen tRNA en mRNA?
- Wat is gedrag van dieren gedragsaanpassing?
- Baanbrekende nieuwe technologie om de wereldwijde zoektocht naar gewasverbetering te versnellen
- Is het ribosoom een plantaardige of dierlijke structuur?
- Begrijpt jouw hond het als je zegt ‘haal de bal’? Een nieuwe studie in Hongarije zegt van wel
- Wie was de naturalist die verantwoordelijk was voor de evolutietheorie?
- Nieuw chemisch hulpmiddel werpt licht op hoe eiwitten elkaar herkennen en met elkaar omgaan
- Wat zijn de drie soorten afval die lichaam produceert?
- Ecologen gebruiken de nieuwste tandheelkundige scantechnologie om jong koraal te bestuderen
- De chemische evolutie van DNA en RNA op de vroege aarde

- Carbonaatstandaarden zorgen voor betere paleothermometers

- Onderzoek verbetert het enzym dat plastic afbreekt
- Zullen sterke en snel wisselende kunstmatige spieren haalbaar zijn?
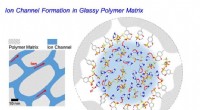
- Wetenschappers vinden een manier om DNA-oppervlaktehybridisatie te versnellen

 Zijn er voorbeelden van potentiële energie?
Zijn er voorbeelden van potentiële energie?  De toekomst zaaien? 'Ark' bewaart zeldzame, bedreigde planten
De toekomst zaaien? 'Ark' bewaart zeldzame, bedreigde planten  De geheimen van het universum ontsluiten
De geheimen van het universum ontsluiten Welke bergen worden geassocieerd met uiteenlopende plaatgrenzen?
Welke bergen worden geassocieerd met uiteenlopende plaatgrenzen?  Hoeveel pond is 82 kg?
Hoeveel pond is 82 kg?  Air France-KLM waarschuwt voor erger nadat virus passagiersaantallen bereikt
Air France-KLM waarschuwt voor erger nadat virus passagiersaantallen bereikt Wat zijn voorbeelden van mechanische energie die worden omgezet in elektrische of warmte -energie?
Wat zijn voorbeelden van mechanische energie die worden omgezet in elektrische of warmte -energie?  Wat gebeurt er met het laserlicht wanneer het satelliet bereikt in het variërende systeem?
Wat gebeurt er met het laserlicht wanneer het satelliet bereikt in het variërende systeem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

