
Wetenschap
Hoeveel gram H 2o wordt geproduceerd als 750 Fe wordt geproduceerd?
Om dit op te lossen, heb je een gebalanceerde chemische vergelijking nodig. Dit is waarom:
* Chemische reacties volgen specifieke verhoudingen: De coëfficiënten in een evenwichtige vergelijking vertellen u de exacte verhoudingen van reactanten en producten.
* We hebben de reactie nodig: We moeten weten welke reactie het ijzer heeft geproduceerd om de waterproductie te achterhalen.
Voorbeeldscenario
Laten we aannemen dat de reactie waarin u geïnteresseerd bent, de reductie van ijzeroxide (Fe₂o₃) is met koolmonoxide (CO):
Fe₂o₃ (s) + 3co (g) → 2fe (s) + 3co₂ (g)
Hoe grams van water te berekenen
1. Balanced vergelijking: Je hebt al een evenwichtige vergelijking voor de reactie.
2. Molaire massa: Vind de molaire massa van Fe (55.845 g/mol) en H₂o (18.015 g/mol).
3. molverhouding: De vergelijking toont aan dat 2 mol Fe wordt geproduceerd voor elke 3 mol CO₂.
4. gram tot mollen: Converteer 750 g Fe naar mol met behulp van de molaire massa van Fe.
5. Moles tot mol: Gebruik de molverhouding van de vergelijking om de mol van de geproduceerde co₂ te vinden.
6. Mols to Grams: Converteer de mol co₂ om te gram met behulp van de molaire massa van CO₂.
Belangrijke opmerking:
* De reactie moet in evenwicht zijn om de juiste molverhoudingen te garanderen.
* De chemische reactie is essentieel voor het bepalen van de waterproductie.
Laat me de specifieke reactie weten die u overweegt, en ik kan u helpen met de berekening!
 Hoeveel moleculen zitten er in een korrel zout?
Hoeveel moleculen zitten er in een korrel zout?  Is waterstofgasdichter dan lucht?
Is waterstofgasdichter dan lucht?  Onderzoekers ontwikkelen dynamische sjablonen die essentieel zijn voor afdrukbare elektronicatechnologie
Onderzoekers ontwikkelen dynamische sjablonen die essentieel zijn voor afdrukbare elektronicatechnologie Wat is een oplosmiddel in experiment?
Wat is een oplosmiddel in experiment?  Hoge precisie chemische vingerafdruk maakt ondubbelzinnige identificatie mogelijk
Hoge precisie chemische vingerafdruk maakt ondubbelzinnige identificatie mogelijk
Hoofdlijnen
- Welke organel is verantwoordelijk voor het aanzetten van energie naar de cel?
- Wat is materie die altijd precies dezelfde compositie heeft geclassificeerd als?
- Wat is het proces waarin onze sensorische receptoren stimuli van de omgeving omzetten in een vorm die kan worden verzonden naar en gebruikt door de hersenen?
- Biogene sedimenten zijn schelpen en skeletten van mariene dierenalgen welke twee voorbeelden dit?
- Bij het vormen van nieuwe DNA -moleculen elke streng van uw handeling als een?
- Temperatuur draagt het meest bij aan de geografische verspreiding van twee gigantische honingbijen
- Wat is de een gevolgtrekking?
- Wat zijn de functies van de twaalfvingerige darm?
- Wat zijn biologisch gebruik?
- Gebrouwen koffiedik biedt duurzaam alternatief voor kledingverf

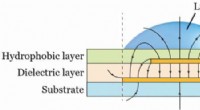
- Hydrogel 3D-print- en patroonvloeistoffen met het condensatorrandeffect (PLEEC)
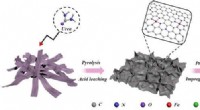
- Wetenschappers stellen nieuwe bifunctionele katalysatoren voor op van biomassa afgeleide koolstof
- Topologiecontrole van menselijke fibroblastcellen monolaag door vloeibaar kristalelastomeer

- Daglichtschadebesparende tijd

 Waar of niet waar Een waterstofbrug wordt voltooid door de overdracht van zijn enige elektron naar een ander element?
Waar of niet waar Een waterstofbrug wordt voltooid door de overdracht van zijn enige elektron naar een ander element?  NASA's Aqua-satelliet volgt Typhoon Nesat op weg naar Taiwan
NASA's Aqua-satelliet volgt Typhoon Nesat op weg naar Taiwan Wat betekent BTB in de wetenschap?
Wat betekent BTB in de wetenschap?  Een sedimentair gesteente wordt verweerd door wind en water de breekt opnieuw in sedimenten als het wordt gecementeerd Welk type zal worden gevormd?
Een sedimentair gesteente wordt verweerd door wind en water de breekt opnieuw in sedimenten als het wordt gecementeerd Welk type zal worden gevormd?  Rollen van celorganellen in mitose
Rollen van celorganellen in mitose Hoe lang duurt het om de zon door een ruimteschip te krijgen?
Hoe lang duurt het om de zon door een ruimteschip te krijgen?  Hoe afrodisiaca werken
Hoe afrodisiaca werken  Hoe behoudt een vacuümkolf zijn energie?
Hoe behoudt een vacuümkolf zijn energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

