
Wetenschap
Wat gebeurt er met deeltjes van materie wanneer een vloeistof van gas verandert?
* Verhoogde afstand: De deeltjes in een vloeistof zijn dicht bij elkaar, maar kunnen bewegen. Wanneer de vloeistof in een gas verandert, verspreiden de deeltjes zich veel verder uit elkaar , veel mobieler worden. Daarom kunnen gassen uitbreiden om hun container te vullen.
* Verhoogde energie: De deeltjes in een gas hebben meer kinetische energie dan die in een vloeistof. Dit betekent dat ze sneller en met meer kracht rondgaan. Deze verhoogde energie is de drijvende kracht achter de staatsverandering.
* Breek intermoleculaire krachten: In een vloeistof worden deeltjes bij elkaar gehouden door intermoleculaire krachten, zoals waterstofbruggen of dipool-dipoolinteracties. Om een gas te worden, moeten deze krachten worden overwonnen . De deeltjes hebben voldoende energie nodig om los te komen van hun buren en onafhankelijk te bewegen.
Denk er zo aan:
Stel je een menigte mensen voor in een drukke kamer (vloeistof). Ze zijn dicht bij elkaar en kunnen een beetje bewegen. Maar als je ze veel energie geeft (warmte), zullen ze zich verspreiden, meer vrij gaan en zelfs de kamer (gas) verlaten.
Hoe gebeurt dit?
Dit proces, bekend als verdamping , kan op twee manieren gebeuren:
* Verdamping: Dit is een langzaam proces dat gebeurt aan het oppervlak van een vloeistof. De deeltjes met de meeste energie ontsnappen aan het oppervlak van de vloeistof en worden gasdeeltjes.
* koken: Dit is een sneller proces dat gebeurt wanneer de vloeistof zijn kookpunt bereikt. Op dit punt wordt voldoende energie aan de vloeistof toegevoegd dat alle deeltjes voldoende energie hebben om de intermoleculaire krachten te overwinnen en gasdeeltjes te worden.
Laat het me weten als je meer wilt weten over een van deze processen!
 Wanneer de oceaan co2 absorbeert pH van waterdruppels Wat is het effect van dit proces?
Wanneer de oceaan co2 absorbeert pH van waterdruppels Wat is het effect van dit proces?  In stikstoffixatie welke 2 moleculen worden geproduceerd, zodat dat in een bruikbare vorm is?
In stikstoffixatie welke 2 moleculen worden geproduceerd, zodat dat in een bruikbare vorm is?  Wetenschappers identificeren bioactieve stoffen in cacaobonen om medicijnen te ontwikkelen om skeletaandoeningen te bestrijden
Wetenschappers identificeren bioactieve stoffen in cacaobonen om medicijnen te ontwikkelen om skeletaandoeningen te bestrijden Hoeveel elektronen zijn er in één neutrale h?
Hoeveel elektronen zijn er in één neutrale h?  Biofysici lossen de ware structuur van het veelbelovende optogenetische eiwit KR2 rhodopsine op
Biofysici lossen de ware structuur van het veelbelovende optogenetische eiwit KR2 rhodopsine op
 NASA vindt extreme regenval in tropische cycloon Kenanga
NASA vindt extreme regenval in tropische cycloon Kenanga Waar komt slechte lucht vandaan?
Waar komt slechte lucht vandaan? Satellietbeelden laten zien dat Willa verdreven is boven Mexico
Satellietbeelden laten zien dat Willa verdreven is boven Mexico Waarde uit riool? Nieuwe technologie maakt varkenshouderij milieuvriendelijker
Waarde uit riool? Nieuwe technologie maakt varkenshouderij milieuvriendelijker Het verlies aan biodiversiteit heeft gevolgen voor samenlevingen en economieën:hoe kan Europa de verspreiding van invasieve soorten het hoofd bieden?
Het verlies aan biodiversiteit heeft gevolgen voor samenlevingen en economieën:hoe kan Europa de verspreiding van invasieve soorten het hoofd bieden?
Hoofdlijnen
- Hoe verwerven cellen voedselergie?
- Coole ideeën voor een 3D-model van DNA
- Wat is een onopvallende milt?
- Klimaatverandering zou de verspreiding van kwallen en ander gelatineus zoöplankton in de Noordelijke IJszee aanzienlijk kunnen veranderen
- Wat stelt het RNA in staat kern te verlaten?
- Waarom onderzoekers geïnteresseerd zijn in het gezond houden van (sommige) koraalduivels
- Invasieve wormen verspreiden zich in arboretumbossen, beperkte effecten tot nu toe
- Selenium beschermt specifieke interneuronen in de hersenen
- Hoe ontwikkelden bacteriën zich voor het eerst op aarde?
- Weet jij de weg naar Berkelium, Californië?

- Structuur van het actieve ingrediënt bismut in Pepto-Bismol onthuld
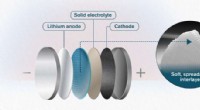
- Een smeerbare tussenlaag kan solid-state batterijen stabieler maken
- Een nieuwe gelelektroforesetechniek voor snelle biomarkerdiagnose via massaspectrometrie

- Synthese van UV-absorbers uit cashewnotenschilvloeistof

 Hoe is de frequentie van de golf gerelateerd aan de tijdsperiode?
Hoe is de frequentie van de golf gerelateerd aan de tijdsperiode?  Moleculen bouwen zoals Tinkertoys? Een baanbrekende studie kan de weg vrijmaken
Moleculen bouwen zoals Tinkertoys? Een baanbrekende studie kan de weg vrijmaken  Hoeveel elektronen worden er in het ethynmolecuul gedeeld?
Hoeveel elektronen worden er in het ethynmolecuul gedeeld?  Thorium supergeleiding:wetenschappers ontdekken nieuwe hoge-temperatuur supergeleider
Thorium supergeleiding:wetenschappers ontdekken nieuwe hoge-temperatuur supergeleider Omdat elektromagnetische energie uit een warmtebron interageert met zijn omgeving die het is?
Omdat elektromagnetische energie uit een warmtebron interageert met zijn omgeving die het is?  Wat gebruiken wetenschappers om een systeem of een object te vertegenwoordigen?
Wat gebruiken wetenschappers om een systeem of een object te vertegenwoordigen?  Hoe de zon werkt
Hoe de zon werkt  Waarom is het fysica belangrijk in radiografie?
Waarom is het fysica belangrijk in radiografie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

