
Wetenschap
Waarom vertonen de elementen die tot een bepaalde groep behoren, vergelijkbaar chemisch gedrag?
* valentie -elektronen: Elementen binnen een groep hebben hetzelfde aantal valentie -elektronen, de elektronen in de buitenste schaal van een atoom. Deze valentie -elektronen zijn degenen die betrokken zijn bij chemische binding.
* Vergelijkbare bindingspatronen: Omdat ze hetzelfde aantal valentie -elektronen hebben, hebben elementen in een groep de neiging om vergelijkbare soorten bindingen te vormen en hebben ze een vergelijkbare reactiviteit. Alle elementen in groep 1 (alkali -metalen) hebben bijvoorbeeld één valentie -elektron, waardoor ze dat elektron gemakkelijk verliezen en +1 ionen vormen.
* Oxidatie stelt: Elementen in een groep vertonen vaak vergelijkbare oxidatietoestanden vanwege hun vergelijkbare valentie -elektronenconfiguraties. Dit betekent dat ze de neiging hebben om op dezelfde manier elektronen te verliezen of te winnen tijdens chemische reacties.
* chemische eigenschappen: De vergelijkbare bindingspatronen en oxidatietoestanden beïnvloeden de chemische eigenschappen van een element rechtstreeks. Elementen in groep 17 (halogenen) zijn bijvoorbeeld allemaal zeer reactieve niet -metalen omdat ze gemakkelijk een elektron krijgen om hun buitenste schaal te voltooien.
Voorbeeld:
* Groep 1 (Alkali metalen): Li, NA, K, RB, CS, FR
* valentie -elektronen: 1
* Chemisch gedrag: Het zijn allemaal zeer reactieve metalen die gemakkelijk hun ene valentie -elektron verliezen om +1 ionen te vormen. Ze reageren krachtig met water en vormen hydroxiden en waterstofgas.
Samenvattend: Het vergelijkbare chemische gedrag van elementen binnen een groep komt voort uit hun gedeelde aantal valentie -elektronen, dat direct hun bindingspatronen, oxidatietoestanden en algemene chemische eigenschappen beïnvloedt.
 In het zicht van New York City, een oerbos wordt geconfronteerd met stormen en zeespiegelstijging
In het zicht van New York City, een oerbos wordt geconfronteerd met stormen en zeespiegelstijging Mineralogie van de aardkorst drijft hotspots voor intraterrestrisch leven
Mineralogie van de aardkorst drijft hotspots voor intraterrestrisch leven Wanneer een object in het zonlicht is, waarom ziet u de kleur ervan?
Wanneer een object in het zonlicht is, waarom ziet u de kleur ervan?  Herinnerend aan de uitbarsting van 1963, Balis ouderen op hun hoede voor een ander
Herinnerend aan de uitbarsting van 1963, Balis ouderen op hun hoede voor een ander Wegenbouwprojecten in het Amazonegebied zouden leiden tot ontbossing van 2,4 miljoen hectare
Wegenbouwprojecten in het Amazonegebied zouden leiden tot ontbossing van 2,4 miljoen hectare
Hoofdlijnen
- Zijn cytoplasma op planten of dieren?
- Hoe werkt het skelet met het ademhalingssysteem?
- Is het mogelijk dat wat micro -organisme twee geslachten heeft?
- Wat is basofiele degeneratie?
- Stijgende zeetemperaturen bedreigen Atlantische populaties van Bulwers-stormvogels
- Genetisch onderzoek werpt licht op hoe de vroegste dieren eruit zagen
- Hoe worden de kleine strengen die in een cel genoemd?
- Welk bloedceltype wordt een polymorf genoemd?
- Wat is Bryophyllum kort uitgelegd?
- Duurzame lijmen van de toekomst blijven niet plakken

- Deze kleine, zelfassemblerende vallen vangen PFAS

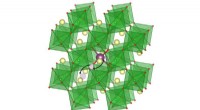
- Lithiumionen stromen door vast materiaal
- Bewijs van waterdraden gemotiveerd door een biologisch waterkanaal

- Bevindingen bieden recept voor fijnafstemming van legeringen voor gebruik bij hoge temperaturen

 Engelennummer 323:Het ontsluiten van de boodschap van groei en harmonie
Engelennummer 323:Het ontsluiten van de boodschap van groei en harmonie  Wat gebeurt er met een vloeibare massa en volume wanneer deze wordt verwarmd of gekoeld?
Wat gebeurt er met een vloeibare massa en volume wanneer deze wordt verwarmd of gekoeld?  Wetenschappers onthullen structuur van aminozuurtransporter die betrokken is bij kanker
Wetenschappers onthullen structuur van aminozuurtransporter die betrokken is bij kanker Ruimtemissie Europa-Japan maakt beelden van Mercurius
Ruimtemissie Europa-Japan maakt beelden van Mercurius Wat wordt materialen met lage weerstand genoemd?
Wat wordt materialen met lage weerstand genoemd?  Hoe kunt u ammoniumchloride en koperoxide scheiden?
Hoe kunt u ammoniumchloride en koperoxide scheiden?  Nieuw voorgesteld multifunctioneel nanomateriaal kan zonne-energie verbeteren, kwantumcomputer
Nieuw voorgesteld multifunctioneel nanomateriaal kan zonne-energie verbeteren, kwantumcomputer Hoe produceren windmolens die kracht produceren, is er geen wind?
Hoe produceren windmolens die kracht produceren, is er geen wind?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

