
Wetenschap
Bevattende element van atoomnummer 53 in pentavalent -toestand?
Waarom jodium pentavalent kan zijn
* Elektronenconfiguratie: Jodium heeft de elektronische configuratie [KR] 4D¹⁰ 5S² 5P⁵. Het kan een stabiel octet bereiken door één elektron te winnen om het jodide -ion te vormen (I⁻). Het kan echter ook elektronen verliezen om positieve oxidatietoestanden te vormen.
* uitgebreid octet: Jodium, als een groot atoom, is geschikt voor meer dan acht elektronen in de valentieschaal. Hierdoor kan het verbindingen vormen waar het een +5 oxidatietoestand heeft.
Voorbeelden van jodium in een pentavalent -toestand
* jodiumzuur (hio₃): In deze verbinding bevindt jodium zich in de +5 oxidatietoestand.
* jodates: Zouten met het jodiumion (io₃⁻), zoals kaliumjodaat (kio₃), hebben ook jodium in de +5 oxidatietoestand.
* jodium pentafluoride (if₅): Deze verbinding heeft jodium met een +5 oxidatietoestand.
Opmerking: Hoewel jodium een pentavalent-toestand kan bereiken, komt het minder vaak voor in vergelijking met de lagere oxidatietoestanden (-1, +1, +3, +7). Dit komt door de toenemende elektronegativiteit van zuurstof, die de neiging heeft om hogere oxidatietoestanden voor jodium te geven.
 Wat zijn fysische en chemische verwering?
Wat zijn fysische en chemische verwering?  Hoe is water dichter dan lavendelolie?
Hoe is water dichter dan lavendelolie?  Nanofractioneringsplatform met parallelle massaspecificatie voor ID-cytochroom-CYP1A2-remmers
Nanofractioneringsplatform met parallelle massaspecificatie voor ID-cytochroom-CYP1A2-remmers Welk type binding houdt de fosfor- en zuurstofatomen bij elkaar in deze molecuul ATP?
Welk type binding houdt de fosfor- en zuurstofatomen bij elkaar in deze molecuul ATP?  Houtfilter verwijdert giftige kleurstof uit water
Houtfilter verwijdert giftige kleurstof uit water
 Klimaatwetenschappelijk rapport cruciaal voor succes van COP26:UN
Klimaatwetenschappelijk rapport cruciaal voor succes van COP26:UN Hoge uitstoot van broeikasgassen uit Siberische binnenwateren
Hoge uitstoot van broeikasgassen uit Siberische binnenwateren Hoe drones explosieve vulkanen kunnen volgen
Hoe drones explosieve vulkanen kunnen volgen De aardbeving van 4 juli zal de Big One niet vertragen. En het zou de aardbevingsspanning kunnen hebben verergerd
De aardbeving van 4 juli zal de Big One niet vertragen. En het zou de aardbevingsspanning kunnen hebben verergerd Wat is het biome met de grootste biodiversiteit?
Wat is het biome met de grootste biodiversiteit?
Hoofdlijnen
- Groeiende weefsels beschrijven in de taal van de thermodynamica
- Wetenschappers hebben fundamentele ontdekkingen gedaan over de manier waarop eigenschappen van embryonale stamcellen worden gecontroleerd
- Dit is wat de wetenschap zegt over het gevoel van dieren
- Gezond of ziek? Kleine celbelletjes kunnen het antwoord bevatten
- Wat is teratogeen?
- Kun jij de vier belangrijkste biomen van BC noemen?
- Chemici ontdekken een sleuteleiwit in de manier waarop lysosomen werken
- Waarom droge massa's organismen?
- Vogelneuronen gebruiken drie keer minder glucose dan zoogdierneuronen
- Vooruitgang van elektrolyse bij hoge temperatuur:water splitsen om energie op te slaan als waterstof

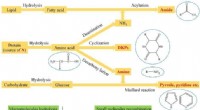
- Een nieuw idee voor het raffineren van biocrude
- Wetenschappers gebruiken gel-polymeer-elektrolyt voor hoogwaardige magnesiumbatterijen

- Beter koper betekent efficiëntere elektromotoren

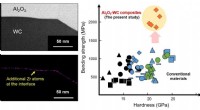
- Zirkonium gebruiken als additief in supersterke composietmaterialen
 Welke van de volgende banen zal een scheikundige waarschijnlijk hebben?
Welke van de volgende banen zal een scheikundige waarschijnlijk hebben?  Kun je de relativiteitstheorie verklaren?
Kun je de relativiteitstheorie verklaren?  De toekomst is nu:vliegende auto komt naar Miami
De toekomst is nu:vliegende auto komt naar Miami Het belangrijkste doel van celdeling is?
Het belangrijkste doel van celdeling is?  Hoe verschillende soorten kennis de groei van nieuwe bedrijven beïnvloeden
Hoe verschillende soorten kennis de groei van nieuwe bedrijven beïnvloeden Nieuwe structurele informatie over functionalisering van gouden nanodeeltjes
Nieuwe structurele informatie over functionalisering van gouden nanodeeltjes Trillingen van sterbeving leiden tot nieuwe schatting voor Melkwegleeftijd
Trillingen van sterbeving leiden tot nieuwe schatting voor Melkwegleeftijd Hoe is vloeistof gerelateerd aan een amorfe vaste stof?
Hoe is vloeistof gerelateerd aan een amorfe vaste stof?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

