
Wetenschap
Hoeveel gram waterstof moet reageren als de reactie 63,5 ammoniak moet produceren?
1. Schrijf de gebalanceerde chemische vergelijking:
N₂ (g) + 3H₂ (g) → 2nh₃ (g)
2. Bepaal de molaire massa ammoniak (NH₃):
* N:14.01 g/mol
* H:1.01 g/mol
* NH₃:14.01 + (3 * 1.01) =17,04 g/mol
3. Bereken de mol ammoniak:
* Mol =massa / molaire massa
* Mol NH₃ =63,5 g / 17,04 g / mol =3,72 mol
4. Gebruik de molverhouding van de gebalanceerde vergelijking om de mol waterstof te vinden:
* De vergelijking toont aan dat 3 mol H₂ reageert om 2 mol NH₃ te produceren.
* Mol h₂ =(3 mol H₂ / 2 mol NH₃) * 3,72 mol NH₃ =5,58 mol H₂
5. Bereken de massa waterstof:
* Massa =mollen * molaire massa
* Massa van H₂ =5,58 mol * 2,02 g/mol = 11.27 g
Daarom moet 11,27 gram waterstof reageren om 63,5 gram ammoniak te produceren.
 Aanpassing regenwoud
Aanpassing regenwoud  Klimaatverandering heeft gevolgen voor de habitat van de Antarctische biodiversiteit
Klimaatverandering heeft gevolgen voor de habitat van de Antarctische biodiversiteit Wat zijn enkele voorbeelden van natuurlijke structuren?
Wat zijn enkele voorbeelden van natuurlijke structuren?  Hoe de delen van een ecosysteem
Hoe de delen van een ecosysteem  Verkenners hebben zojuist de diepste grot van Australië ontdekt. Een hydrogeoloog legt uit hoe ze ontstaan
Verkenners hebben zojuist de diepste grot van Australië ontdekt. Een hydrogeoloog legt uit hoe ze ontstaan
Hoofdlijnen
- Hoe vissen tegelijkertijd geluiden horen en maken
- Wat is het verschil tussen antebrachium en brachium?
- Hoe wordt het ene geslacht groter dan het andere?
- Is de pijnappelklier lichtste orgel op het lichaam?
- Wat is uniek aan chloroplast en mitochondria?
- Hoe werkt de kernbeheersingsfuncties van het leven?
- Hoe een dodelijke schimmel het immuunsysteem ontwijkt
- Behoud oproep aan zaagviskwekerij
- Hoe voedingskeuze de levensduur van fruitvliegjes beïnvloedt
- Onderzoekers werpen nieuw licht op detectie van griep

- Titaanatoom dat op twee plaatsen tegelijk in kristal bestaat en de oorzaak is van een ongewoon fenomeen

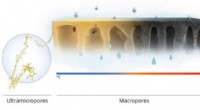
- Brandmembranen voor moleculair zeven
- Techniek geeft gedetailleerd inzicht in hoe bepaalde polymeren worden gevormd, antwoorden ontsluiten over kiemvorming

- Het oplossen van een 75 jaar oud mysterie kan een nieuwe bron van landbouwmest opleveren

 Wat gebeurt er wanneer opgeloste mineralen worden afgezet in kleine ruimtes tussen de sedimenten?
Wat gebeurt er wanneer opgeloste mineralen worden afgezet in kleine ruimtes tussen de sedimenten?  Welke drie dingen moet je altijd doen bij het hanteren van zuur of alkali in een lab?
Welke drie dingen moet je altijd doen bij het hanteren van zuur of alkali in een lab?  Waarom oorlog een mannenspel is
Waarom oorlog een mannenspel is Een hart van goud:beter weefselherstel na een hartaanval (update)
Een hart van goud:beter weefselherstel na een hartaanval (update) Canada, Amerikaanse hittegolf op steroïden door klimaatverandering, zeggen experts
Canada, Amerikaanse hittegolf op steroïden door klimaatverandering, zeggen experts Is hout een efficiënte geleider van warmte en energie?
Is hout een efficiënte geleider van warmte en energie?  Hoeveel druppels water is gelijk aan één vloeiende ounce?
Hoeveel druppels water is gelijk aan één vloeiende ounce?  Kan kleine kracht een groter koppel uitoefenen?
Kan kleine kracht een groter koppel uitoefenen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

