
Wetenschap
Wat is de niet -verkorte elektronenconfiguratie van broom?
De niet -verkorte elektronenconfiguratie van broom is:
1S² 2S² 2P⁶ 3S² 3P⁶ 4S² 3D¹⁰ 4P⁵
Hier is hoe u dit kunt begrijpen:
* 1S²: Het eerste energieniveau (n =1) heeft één subbleevel (s) met twee elektronen.
* 2s² 2p⁶: Het tweede energieniveau (n =2) heeft twee abuuten (S en P) met in totaal acht elektronen.
* 3S² 3P⁶ 4S² 3D¹⁰ 4P⁵: De derde en vierde energieniveaus (n =3 en n =4) hebben in totaal 35 elektronen verdeeld over hun abuusplaatsen.
Vergeet niet dat bromine (BR) een halogeen is, wat betekent dat het 7 valentie -elektronen heeft (in het 4P -abuuste).
 Een kluizenaarkrab vinden
Een kluizenaarkrab vinden Rijke landen lopen ver achter met klimaatbelofte van 100 miljard dollar:studie
Rijke landen lopen ver achter met klimaatbelofte van 100 miljard dollar:studie Welke seizoenen hebben overstromingen?
Welke seizoenen hebben overstromingen?  Onderzoekers tonen aan dat reputatieproblemen mensen kunnen aanmoedigen om deel te nemen aan echte 'publieke goede'-programma's
Onderzoekers tonen aan dat reputatieproblemen mensen kunnen aanmoedigen om deel te nemen aan echte 'publieke goede'-programma's  Als het om klimaatverandering gaat, Australische mijnbouwreuzen zijn medeplichtig aan de misdaad
Als het om klimaatverandering gaat, Australische mijnbouwreuzen zijn medeplichtig aan de misdaad
Hoofdlijnen
- Wat zijn anti -lichamen en antigeen?
- Hoe wordt de buitenste bedekking van spier genoemd?
- Hoe definieer je haat?
- Waarom is water van levensbelang?
- Wat zijn voorbeelden van één gram?
- Waarom vissen naar beneden kijken als ze zwemmen
- Wat zijn enkele analogieën voor Golgi -apparaten en flagellum?
- Groot met vloeistof gevuld organel in volwassen plantencellen?
- Wat zijn waterhozen en hoe ontstaan ze?
- Gerecycled beton kan een duurzame manier zijn om puin van stortplaatsen te houden

- Verdunning detecteren:nieuwe experimentele en theoretische benaderingen duiken in de pool van organellen van membranen

- Chemici vinden een nieuwe tool om enzymen te begrijpen:Google
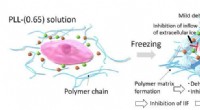
- Nieuwe inzichten bevriezen de mechanismen om biologische materialen veilig te bewaren
- Vissen naar één slechte cel uit triljoenen goede

 Wat is de langste enkele dubbele of drievoudige covalente binding tussen dezelfde twee atomen?
Wat is de langste enkele dubbele of drievoudige covalente binding tussen dezelfde twee atomen?  Voorbeelden van sensorische adaptatie
Voorbeelden van sensorische adaptatie  De behoefte aan progressieve nationale verhalen
De behoefte aan progressieve nationale verhalen Auto's:overgang van lockdown is een splitsing in de weg - hier zijn twee mogelijke uitkomsten voor toekomstige reizen
Auto's:overgang van lockdown is een splitsing in de weg - hier zijn twee mogelijke uitkomsten voor toekomstige reizen Welke toestand heeft moleculen in een zeer losjes pack?
Welke toestand heeft moleculen in een zeer losjes pack?  Hoe bananen kunnen worden gebruikt om de plasticafvalcrisis te bestrijden
Hoe bananen kunnen worden gebruikt om de plasticafvalcrisis te bestrijden  Hoeveel golven gaan voorbij een punt in 1 seconde als de frequentie 5Hz is?
Hoeveel golven gaan voorbij een punt in 1 seconde als de frequentie 5Hz is?  Oude SpaceX-capsule levert nieuwe bemanning aan ruimtestation
Oude SpaceX-capsule levert nieuwe bemanning aan ruimtestation
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

