
Wetenschap
Wat zijn de producten van reactie van kaliumchloraat?
Hier zijn de twee belangrijkste scenario's:
1. Ontleding met warmte:
* zonder katalysator: Wanneer kaliumchloraat wordt verwarmd, ontleedt het om kaliumchloride (KCL) te vormen en zuurstofgas (o₂) .
* 2kclo₃ → 2kcl + 3o₂
* met een katalysator: Als een katalysator zoals mangaandioxide (MNO₂) aanwezig is, treedt de reactie op bij een lagere temperatuur en produceert dezelfde producten:
* 2kclo₃ → 2kcl + 3o₂
2. Ontleding met een reductiemiddel:
* Wanneer kaliumchloraat reageert met een reductiemiddel, zoals zwavel, zijn de producten kaliumchloride (KCL) en zwaveldioxide (So₂) .
* 2kclo₃ + s → 2kcl + so₂
Belangrijke opmerking: De ontleding van kaliumchloraat is een zeer exotherme reactie, wat betekent dat het veel warmte vrijgeeft. Dit maakt het belangrijk om deze chemische stof met voorzichtigheid af te handelen, vooral bij het verwarmen.
 Natte vuurrook in wolken onderzoeken:kan water de opwarming van de aarde versterken?
Natte vuurrook in wolken onderzoeken:kan water de opwarming van de aarde versterken? Hoe klimaatverandering de stroom van de Colorado-rivier verminderde
Hoe klimaatverandering de stroom van de Colorado-rivier verminderde  Hoe noem je persoon die de aarde studeert?
Hoe noem je persoon die de aarde studeert?  Gebeiteld in steen? Kooldioxide omzetten in steen, voor goed
Gebeiteld in steen? Kooldioxide omzetten in steen, voor goed Antarctica is niet langer de koele plaats die het vroeger was voor zijn aan kou aangepaste vissen. Dus wat is er veranderd?
Antarctica is niet langer de koele plaats die het vroeger was voor zijn aan kou aangepaste vissen. Dus wat is er veranderd?
Hoofdlijnen
- Wat is de mobiele organisatie van Archaea?
- Bacterieel controlemechanisme voor aanpassing aan veranderende omstandigheden
- Wat is een niet -voorbeeld van chromosoom?
- De studie van hoe omgevingsfactoren de expressiegenen beïnvloeden zonder DNA te veranderen, staat bekend als?
- Wat zorgt ervoor dat vliegen aanvallen?
- 10 echt slimme mensen die echt domme dingen deden
- In de longen gemodificeerde eiwitten bieden aanwijzingen voor de biologische functies van broom
- Het co-evoluerende web van het leven als een netwerk begrijpen
- Wat zijn de twee functies van de huid?
- Zelf-assemblerende eiwitfilamenten die helemaal opnieuw zijn ontworpen en gebouwd

- Micro-/nano-architecturen in MOF-membraan versnellen olie-waterscheiding

- Onderzoekers meten elektronenemissie om het begrip van lasergebaseerd 3D-printen van metaal te verbeteren

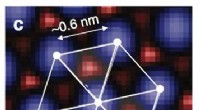
- Het oppervlak van lithiumtitanaat scannen
- Stralingsdetecterend plastic krijgt ingrediënt om helder te blijven

 Hoe verschillen handtekeningen van heterotrofen bij het verkrijgen van energie?
Hoe verschillen handtekeningen van heterotrofen bij het verkrijgen van energie?  Het vinden van nieuwe soorten 2D-materiaaldefecten kan betere elektronica mogelijk maken
Het vinden van nieuwe soorten 2D-materiaaldefecten kan betere elektronica mogelijk maken Onderzoekers rapporteren bevindingen over de controle van celdeling
Onderzoekers rapporteren bevindingen over de controle van celdeling Duurzaamheid versus recycleerbaarheid:doelen stellen bij het verduurzamen van elektronica
Duurzaamheid versus recycleerbaarheid:doelen stellen bij het verduurzamen van elektronica Gepersonaliseerde zweetsensor meet betrouwbaar de bloedglucose zonder vingerprikken
Gepersonaliseerde zweetsensor meet betrouwbaar de bloedglucose zonder vingerprikken Is de aarde in het midden van het zonnestelsel?
Is de aarde in het midden van het zonnestelsel?  Wanneer u een licht- of ander elektrisch apparaatcircuit inschakelt?
Wanneer u een licht- of ander elektrisch apparaatcircuit inschakelt?  Een langverwachte modernisering van keramische productiemethoden
Een langverwachte modernisering van keramische productiemethoden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

