
Wetenschap
Wat is de concentratie van een oplossing van 450 ml die ijzerchloride van 200 gram bevat?
Hier leest u hoe u de concentratie van de ijzerchloride -oplossing kunt berekenen:
1. Converteer grams naar mollen:
* Vind de molaire massa van ijzerchloride (Fecl₃):
* Fe:55.845 g/mol
* Cl:35.453 g/mol
* Fecl₃:55.845 + (35.453 x 3) =162.204 g/mol
* Verdeel de massa ijzerchloride door zijn molaire massa:
* 200 g / 162.204 g / mol =1.233 mol
2. Converteer ML naar liters:
* Verdeel het volume in ml door 1000:
* 450 ml / 1000 ml / l =0,45 l
3. Bereken de concentratie (molariteit):
* Molariteit (M) wordt gedefinieerd als mol opgeloste stof per liter oplossing:
* M =mol opgeloste oplossing
* M =1,233 mol / 0,45 l =2,74 m
Daarom is de concentratie van de ijzerchloride -oplossing 2,74 m (molair).
 Hoe kunnen principes worden gebruikt om menselijke eigenschappen te bestuderen?
Hoe kunnen principes worden gebruikt om menselijke eigenschappen te bestuderen?  Enorme en giftige algenbloei bedreigt kusten van Florida met weer een verloren zomer
Enorme en giftige algenbloei bedreigt kusten van Florida met weer een verloren zomer Een voorbeeld van een landfunctie gevormd door riviererosie is?
Een voorbeeld van een landfunctie gevormd door riviererosie is?  Canada verbiedt plastic voor eenmalig gebruik vanaf 2021
Canada verbiedt plastic voor eenmalig gebruik vanaf 2021 Wat gaat er helemaal rond de aarde, vooral door water dat bekend staat?
Wat gaat er helemaal rond de aarde, vooral door water dat bekend staat?
Hoofdlijnen
- Onderzoeker schetst hoe de sensorische systemen van walvissen zijn geëvolueerd door middel van beeldtechnologie
- Hoe vleermuizen evolueerden om kanker te voorkomen
- Welke structuren gaan uit elkaar tijdens mitose en creëren spil?
- Is een atoom een multicellulair organisme of eencellulair organisme?
- Het is onwaarschijnlijk dat de jacht op trofeeën de evolutie beïnvloedt
- Nieuw mechanisme verduidelijkt hoe cellen migreren
- Waarom je meer sympathie zou moeten hebben voor zeemeeuwen en hoe je kunt voorkomen dat ze je fiches stelen
- Hoe cellen kunstmatige ingrediënten 'lezen' die in een genetisch recept worden gegooid
- Welk voorbeeld toont een organisme dat homeostase handhaaft A. Een kip leggen eieren B.A persoon die zweten op een warme dag c.a hagedis veranderende kleur om predatord te voorkomen. Bacterie die in twee gaat?
- Ervoor zorgen dat broccolispruiten hun kankerbestrijdende stoffen behouden

- RNA aanvallen met medicijnen met kleine moleculen

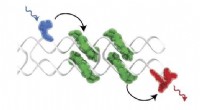
- Leren van fotosynthese:synthetische circuits kunnen lichtenergie oogsten
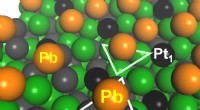
- Ultrastabiel, selectieve katalysator voor propaandehydrogenering ontwikkeld
- Door zonlicht en afvalwaternitraat te combineren om 's werelds nummer 2 chemisch te maken

 Inside story:hoe de Russen de e-mails van de Democraten hackten
Inside story:hoe de Russen de e-mails van de Democraten hackten  Zwarte psychiatrische patiënten zwaar getroffen door COVID-19, sociaal onrecht:we zaten al op een breekpunt
Zwarte psychiatrische patiënten zwaar getroffen door COVID-19, sociaal onrecht:we zaten al op een breekpunt Leg uit waarom grote keien aanwezig zijn in steile bergen stromen?
Leg uit waarom grote keien aanwezig zijn in steile bergen stromen?  Nanodeeltjes werken samen om tumoren te detecteren en te behandelen
Nanodeeltjes werken samen om tumoren te detecteren en te behandelen Welke twee fundamentele tendensen in de natuur lijken het reactieproces te beïnvloeden?
Welke twee fundamentele tendensen in de natuur lijken het reactieproces te beïnvloeden?  Wat zijn gratis trillingen van een lichaam?
Wat zijn gratis trillingen van een lichaam?  Wat betekent donkere energie?
Wat betekent donkere energie?  Model onthult hoe plasma van superstormen de nabije aardse ruimte beïnvloedt
Model onthult hoe plasma van superstormen de nabije aardse ruimte beïnvloedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

