
Wetenschap
Is de ionische binding sterker in NaCl of calciumcarbonaat?
* Laaddichtheid: Natriumchloride (NaCl) bestaat uit Na+ en clionen. Beide ionen hebben een enkele lading (+1 en -1). Calciumcarbonaat daarentegen heeft Ca2+ en Co32-ionen, met dubbele ladingen. Hoewel hogere ladingen leiden tot sterkere attracties, speelt de grootte van de ionen ook een rol.
* ionische grootte: Natrium- en chlorideionen zijn relatief klein in vergelijking met calcium- en carbonaationen. Kleinere ionen hebben een hogere ladingsdichtheid, wat betekent dat de lading geconcentreerd is over een kleiner gebied, wat leidt tot sterkere elektrostatische attracties.
* roosterstructuur: NaCl heeft een eenvoudige kubieke roosterstructuur, die een efficiënte verpakking van de ionen mogelijk maakt en elektrostatische attracties maximaliseert. Calciumcarbonaat heeft een complexere structuur, die de algehele sterkte van de ionische bindingen vermindert.
Samenvattend:
* Hogere ladingsdichtheid in NaCl vanwege kleinere ionen.
* eenvoudiger roosterstructuur in NaCl, waardoor nauwere verpakking mogelijk is.
Deze factoren dragen bij aan sterkere ionische bindingen in NaCl in vergelijking met calciumcarbonaat.
 De 12 vragen die aardwetenschappers de komende 10 jaar zouden moeten stellen
De 12 vragen die aardwetenschappers de komende 10 jaar zouden moeten stellen Wat probeerden de romantici na te denken over de natuurlijke wereld?
Wat probeerden de romantici na te denken over de natuurlijke wereld?  Drie redenen waarom orkaan Ian een groot overstromingsgevaar vormt voor Florida:een meteoroloog legt uit
Drie redenen waarom orkaan Ian een groot overstromingsgevaar vormt voor Florida:een meteoroloog legt uit Hoe planten luchtwortels maken
Hoe planten luchtwortels maken  Heeft de hoeveelheid mineralen invloed op de groei van de planten?
Heeft de hoeveelheid mineralen invloed op de groei van de planten?
Hoofdlijnen
- Microben reizen door de lucht; Het zou goed zijn om te weten hoe en waar
- Wat gebruiken organismen om te werken en veranderen?
- Bijen zijn verbazingwekkend goed in het nemen van beslissingen – en ons computermodel legt uit hoe dat mogelijk is
- Wat hondeneigenaren moeten weten over leptospirose
- Op de loer in genomische schaduwen:hoe gigantische virussen de evolutie van algen voeden
- Waarom zijn decomposers essentieel voor de creatie?
- Welke soorten dieren eten balpythons?
- Twee nieuwe ontdekkingen werpen licht op het mysterie van hoe cellen met stress omgaan
- Grenzen van het uithoudingsvermogen als marathonsterren geen tijd meer hebben
- Wetenschappers ontdekken hoe malariaparasieten suiker importeren
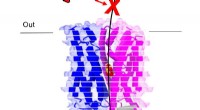
- Afbeeldingen van onzichtbare gaten in cellen kunnen onderzoek op gang brengen

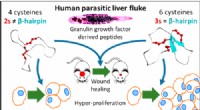
- Een molecuul geproduceerd door een Thaise leverparasiet zou de oplossing kunnen zijn voor die niet-genezende wonden
- Computers strijden mee tegen COVID-19

- Nieuw retroreflecterend materiaal kan worden gebruikt in nachtelijke, van kleur veranderende verkeersborden

 Waarom verandert het uiterlijk van de maan?
Waarom verandert het uiterlijk van de maan?  Combineren van DNA en fossiel bewijs om te begrijpen hoe boommarters evolueerden tijdens de ijstijd
Combineren van DNA en fossiel bewijs om te begrijpen hoe boommarters evolueerden tijdens de ijstijd Wat zijn feiten over de bosbodem?
Wat zijn feiten over de bosbodem?  Online simulatiespel maakt onderzoek naar grafeen beschikbaar voor het publiek
Online simulatiespel maakt onderzoek naar grafeen beschikbaar voor het publiek Wetenschappers ontdekken aanwijzing in het geval van het ontbrekende zilver
Wetenschappers ontdekken aanwijzing in het geval van het ontbrekende zilver Kleinste transistor ter wereld schakelt stroom met een enkel atoom in vast elektrolyt
Kleinste transistor ter wereld schakelt stroom met een enkel atoom in vast elektrolyt Welke vorm van energie zou een zonnekoker gebruiken?
Welke vorm van energie zou een zonnekoker gebruiken?  Heeft endotherm een hoge of lage activeringsenergie?
Heeft endotherm een hoge of lage activeringsenergie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

