
Wetenschap
Reageren sterke zuren of basen gemakkelijker met materialen dan zwakke en bases?
* Sterke zuren en basen dissociëren volledig in oplossing: Dit betekent dat ze al hun waterstofionen (H+) of hydroxide-ionen (OH-) in de oplossing vrijgeven. Deze hoge concentratie reactieve ionen maakt ze zeer reactief.
* Zwakke zuren en basen dissociëren gedeeltelijk: Ze geven alleen een klein deel van hun waterstof- of hydroxide -ionen vrij, wat resulteert in een lagere concentratie reactieve ionen en dus een langzamere reactiesnelheid.
Denk er op deze manier aan:
* Sterke zuren/basen zijn als een grote menigte mensen: Ze hebben veel mensen klaar om te communiceren en een reactie te veroorzaken.
* Zwakke zuren/basen zijn als een kleine groep mensen: Ze hebben minder individuen om te communiceren, waardoor de reactie langzamer en minder krachtig wordt.
Voorbeelden:
* sterk zuur (HCl) op metaal: HCL reageert snel met metalen zoals zink om waterstofgas te produceren, vaak met krachtig borrelen en warmteafgifte.
* zwak zuur (azijnzuur) op metaal: Azijnzuur (azijn) reageert veel langzamer met metalen en de reactie is minder merkbaar.
Belangrijke opmerking: Hoewel sterke zuren en basen gemakkelijker reageren, zijn ze niet altijd de gevaarlijkste. De concentratie van het zuur of de basis speelt een belangrijke rol bij het bepalen van de ernst van de reactie. Een sterk geconcentreerd zwak zuur kan net zo gevaarlijk zijn als een verdund sterk zuur.
 Hoe zijn chemicl -bindingen belangrijk bij het metabolisme?
Hoe zijn chemicl -bindingen belangrijk bij het metabolisme?  Wat gebruikt gas in huis?
Wat gebruikt gas in huis?  Waarom gebruik je geconcentreerd salpeterzuur bij het bereiden van ammonium ijzersulfaat?
Waarom gebruik je geconcentreerd salpeterzuur bij het bereiden van ammonium ijzersulfaat?  Hoe helpen wetenschappelijke tests te bepalen naar eigenschappen van inhoud?
Hoe helpen wetenschappelijke tests te bepalen naar eigenschappen van inhoud?  Een atoom met vier protonen en zes neutronen is elektrisch neutraal als het ?
Een atoom met vier protonen en zes neutronen is elektrisch neutraal als het ?
 Kabelbacteriën kunnen de uitstoot van broeikasgassen door de rijstteelt drastisch verminderen
Kabelbacteriën kunnen de uitstoot van broeikasgassen door de rijstteelt drastisch verminderen Onderzoekers onthullen stratosferisch luchtintrusieproces
Onderzoekers onthullen stratosferisch luchtintrusieproces Nieuwe bevindingen over lachgasemissies van noordelijke bomen verrasten wetenschappers
Nieuwe bevindingen over lachgasemissies van noordelijke bomen verrasten wetenschappers Waar is de sneeuw? Klimaatverandering heeft invloed op het skiraceseizoen
Waar is de sneeuw? Klimaatverandering heeft invloed op het skiraceseizoen  Hoe soorten in het wild omgaan met de risico's en voordelen van het delen van ruimte met mensen
Hoe soorten in het wild omgaan met de risico's en voordelen van het delen van ruimte met mensen
Hoofdlijnen
- Wat betekent de opstelling van nucleotiden in cellen?
- Waarom kunnen bacteriën zo snel evolueren?
- Waarom zijn de buitenste bedekkingen belangrijk voor beweging in veel ongewervelde dieren?
- Hoe worden de individuele zakjes gevormd door het binnenmembraan genoemd?
- Wat zijn de kenmerken die alle bacteriën gemeenschappelijk hebben?
- Wat is er in de fysiologie?
- Wat zijn suiker en fosfaat?
- Welke soorten epitheelcellen scheiden het slijm uit?
- Welke voortplantingsstructuren worden geproduceerd in de eierstokken van planten?
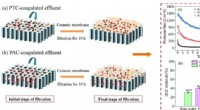
- Polytitaniumchloride pre-coagulatie voor vervuilingscontrole van keramisch membraan
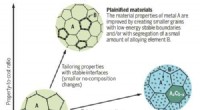
- Verduidelijking belooft veel goeds voor het verbeteren van de duurzaamheid van materialen
- ORNL onderzoekt complexe uraniumoxiden met hulp van CADES-bronnen

- Waterafstotend materiaal werpt af als een slang bij beschadiging

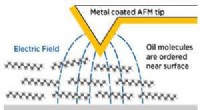
- Weer een stap dichter bij afstembare vloeistoffen
 Het gebruik van glowsticks in vallen verhoogt de vangst van amfibieën in studie aanzienlijk
Het gebruik van glowsticks in vallen verhoogt de vangst van amfibieën in studie aanzienlijk Wat is de industrie voor het meten en controleren van apparaten?
Wat is de industrie voor het meten en controleren van apparaten?  Welk zout wordt geproduceerd wanneer koperoxide reageert met zoutzuur?
Welk zout wordt geproduceerd wanneer koperoxide reageert met zoutzuur?  Wat is het atoom als de massa 2,67x10-24 g is?
Wat is het atoom als de massa 2,67x10-24 g is?  Is er een boom met doornen?
Is er een boom met doornen?  De meeste grotere dieren vervoeren zuurstof in rode bloedcel. Wat zijn de voordelen hiervan?
De meeste grotere dieren vervoeren zuurstof in rode bloedcel. Wat zijn de voordelen hiervan?  Hoe beïnvloedt bergbuilding de atmosfeerbiosfeer en hydrosfeer?
Hoe beïnvloedt bergbuilding de atmosfeerbiosfeer en hydrosfeer?  Spectrale bibliotheek onthult hoe boreale bomen zonnestraling reflecteren
Spectrale bibliotheek onthult hoe boreale bomen zonnestraling reflecteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

