
Wetenschap
Waarom gebruik je geconcentreerd salpeterzuur bij het bereiden van ammonium ijzersulfaat?
1. Oxidatie van ijzer:
* De primaire rol van het zuur is om ijzer te oxideren (Fe) naar zijn +3 oxidatietoestand, die ijzerionen vormt (Fe³⁺). Dit is cruciaal omdat ammoniumferrisch sulfaat (NH₄) ₃fe (So₄) ₃ ijzer bevat in de +3 -toestand.
* Geconcentreerd zwavelzuur is een sterk oxidatiemiddel, in staat om te reageren met ijzermetaal. Deze reactie produceert ijzer (III) sulfaat, een belangrijk onderdeel van ammoniumferrisch sulfaat.
2. Reactie met ammoniumsulfaat:
* Na de oxidatie bevat de oplossing ijzer (III) sulfaat (Fe₂ (So₄) ₃).
* Deze oplossing wordt vervolgens gemengd met ammoniumsulfaat ((NH₄) ₂SO₄).
* De reactie tussen ijzer (III) sulfaat en ammoniumsulfaat produceert ammonium ijzersulfaat.
Waarom geen salpeterzuur?
* Hoewel salpeterzuur ook een oxidatiemiddel is, is het niet zo geschikt voor deze specifieke voorbereiding:
* Tikstofzuur produceert stikstofoxiden (NOx) als bijproducten, die de reactie kunnen bemoeilijken en de zuivering van het eindproduct moeilijker kunnen maken.
* Het gebruik van salpeterzuur kan leiden tot de vorming van ongewenste nitraten, die moeilijk te verwijderen kunnen zijn.
Samenvattend:
* Geconcentreerd zwavelzuur is het voorkeursreagens voor het bereiden van ammoniumferrisch sulfaat omdat het ijzer efficiënt oxideert in de +3 toestand en de vorming van ongewenste bijproducten vermijdt.
* Tikstofzuur wordt meestal niet gebruikt vanwege de neiging om NOx en nitraten te produceren, die het proces bemoeilijken.
 Onderzoekers pionieren met machine learning om chemische ontdekkingen te versnellen, afval verminderen
Onderzoekers pionieren met machine learning om chemische ontdekkingen te versnellen, afval verminderen Vergelijk de magnitudes van dipool-dipoolkrachten tussen deeltjes een stof in vloeibare toestand met gasvormige toestand?
Vergelijk de magnitudes van dipool-dipoolkrachten tussen deeltjes een stof in vloeibare toestand met gasvormige toestand?  Hoe pasteurisatie werkt
Hoe pasteurisatie werkt  Ionische zonnecel kan on-demand waterontzilting bieden;
Ionische zonnecel kan on-demand waterontzilting bieden; Waar is het kookpunt en het vriespunt voor?
Waar is het kookpunt en het vriespunt voor?
 Wat is de functie van een top in een blad?
Wat is de functie van een top in een blad?  Duitse onderzoekers achterhalen hoe pils zich voor het eerst ontwikkelde in Beieren
Duitse onderzoekers achterhalen hoe pils zich voor het eerst ontwikkelde in Beieren  Silencing science tracker uitgebreid met acties van de staat en de lokale overheid
Silencing science tracker uitgebreid met acties van de staat en de lokale overheid Sedimentkern uit sluisvijver bevat bewijs voor aardbeving in New England in 1755
Sedimentkern uit sluisvijver bevat bewijs voor aardbeving in New England in 1755 Welke dieren leven op de pelagische zone?
Welke dieren leven op de pelagische zone?
Hoofdlijnen
- Wanneer kan het fenotype je genotype van een eigenschap vertellen?
- Wat zijn enkele basistheorieën over de biologie?
- Hoeveel zintuigen heeft een mens?
- Wat is een gedrag dat genetisch bepaald en niet kan worden gewijzigd?
- Wetenschappers onthullen hoe een weinig bekende amoebe een bacterie overspoelde om fotosynthetisch te worden
- In welke periode geloven wetenschappers dat de tuinbouw begint?
- Welke groep micro -organismen bio -energetisch enzymsysteem?
- Cellen in de bladeren van planten bevatten gespecialiseerde structuren die chloroplasten worden genoemd, hoe zijn gerelateerd aan functiebladcellen?
- Hoe zijn de takken van de wetenschap met elkaar verbonden?
- Onderzoeker ontwikkelt methode om fundamentele architectuur van polymeren te veranderen

- Bio-ingenieurs ontwikkelen zich snel, op speeksel gebaseerde detectietest voor marihuana

- Met de steigermethode kunnen biochemici eiwitten in opmerkelijk detail zien

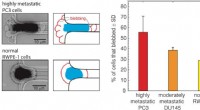
- Nieuwe techniek belooft verbeterde detectie van uitgezaaide prostaatkanker
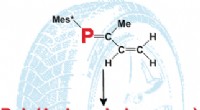
- Een chemisch functionele fosforversie van natuurlijk rubber
 Een golf heeft een snelheid van 300 ms en een golflengte van 3 m. Wat is de frequentiegolf?
Een golf heeft een snelheid van 300 ms en een golflengte van 3 m. Wat is de frequentiegolf?  Wie heeft de schuld toen iCloud werd 'gehackt':jij of Apple?
Wie heeft de schuld toen iCloud werd 'gehackt':jij of Apple?  Zoutere waterwegen creëren gevaarlijke chemische cocktails
Zoutere waterwegen creëren gevaarlijke chemische cocktails Hoe de axiale belasting te berekenen
Hoe de axiale belasting te berekenen  Gigantische hagel in Argentinië heeft mogelijk wereldrecord gebroken
Gigantische hagel in Argentinië heeft mogelijk wereldrecord gebroken Wat zijn 3 soorten gletsjerbewegingen?
Wat zijn 3 soorten gletsjerbewegingen?  IMERG toont verwoestende regenval boven Oost-Afrika
IMERG toont verwoestende regenval boven Oost-Afrika Verstrengelde fotonen genereren met niet-lineaire meta-oppervlakken
Verstrengelde fotonen genereren met niet-lineaire meta-oppervlakken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

