
Wetenschap
Wat gebeurt er wanneer hydrofluorzuuroplossing wordt gereageerd met een lithiumhydroxide -oplossing?
Hier is de evenwichtige chemische vergelijking:
hf (aq) + liOH (aq) → lif (aq) + h₂o (l)
Verklaring:
* hydrofluorinezuur (HF) is een zwak zuur, wat betekent dat het slechts gedeeltelijk in oplossing is ioniseert.
* lithiumhydroxide (liOH) is een sterke basis, wat betekent dat het volledig ioniseert in oplossing.
* Wanneer de twee oplossingen worden gemengd, reageren de waterstofionen (H⁺) van de HF met de hydroxide -ionen (OH⁻) van de LIOH om water te vormen (H₂o).
* De resterende ionen, lithium (Li⁺) en fluoride (F⁻), combineren om lithiumfluoride (LIF) te vormen, die in de oplossing blijft opgelost.
Belangrijke opmerking:
Hoewel deze reactie een standaardneutralisatiereactie is, is het cruciaal om te onthouden dat hydrofluorzuur zeer corrosief en gevaarlijk is. Het kan ernstige brandwonden en zelfs de dood veroorzaken als het niet goed wordt behandeld. Het is essentieel om de juiste veiligheidsmaatregelen en beschermende uitrusting te gebruiken bij het werken met hydrofluorinezuur.
 Efficiëntie in fotokatalyse bleek plaatsgevoelig te zijn
Efficiëntie in fotokatalyse bleek plaatsgevoelig te zijn Wat is het gebruik van thermohardende kunststoffen?
Wat is het gebruik van thermohardende kunststoffen?  Sugar lost op in water sneller dan zoutwetenschappelijke projecten
Sugar lost op in water sneller dan zoutwetenschappelijke projecten  Chemici suggereren een nieuwe manier om steroïde-analogen te synthetiseren
Chemici suggereren een nieuwe manier om steroïde-analogen te synthetiseren Wat is de relatie tussen reactanten en producten in chemische reacties?
Wat is de relatie tussen reactanten en producten in chemische reacties?
 Bosbranden in Australië leiden tot ongekende klimaatdesinformatie
Bosbranden in Australië leiden tot ongekende klimaatdesinformatie Wat is de relatie tussen ecologisch en opvolgingsevenwicht in een ecosysteem?
Wat is de relatie tussen ecologisch en opvolgingsevenwicht in een ecosysteem?  Geef de shiraz door, alsjeblieft:hoe de Australische wijnindustrie zich kan aanpassen aan klimaatverandering
Geef de shiraz door, alsjeblieft:hoe de Australische wijnindustrie zich kan aanpassen aan klimaatverandering NASA ziet orkaan Max aan land komen en verzwakken
NASA ziet orkaan Max aan land komen en verzwakken Naar de bodem van de Antarctische ijsplaat smelten
Naar de bodem van de Antarctische ijsplaat smelten
Hoofdlijnen
- Wat is een voorbeeld van een niet -schadelijke bacteriën?
- Welke objecten zetten zonlicht om in suikers?
- In welk biome bevindt Maleisië zich?
- Exploderende kamikazebacteriën:hoe een paar ‘soldaatcellen’ de bevolking virulentie verlenen door zichzelf op te offeren
- De nanoscopische structuur die onze genen opsluit
- Wat is het weefsel voor zenuwcel?
- Wat zijn het verschil dat wetenschap wordt geprojecteerd?
- Hoe kunstmatige intelligentie de illegale handel in wilde dieren kan helpen voorkomen
- Beperkingen Enzymen die worden gebruikt in DNA-vingerafdrukken
- Een elektrische benadering met één molecuul voor aminozuurdetectie en chiraliteitsherkenning
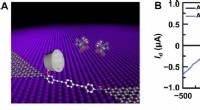
- Afluisteren van afzonderlijke moleculen met licht door het gebabbel opnieuw af te spelen

- Sneller polymeerstructuren produceren – twee processen in één machine

- Hoe kooldioxide uit de lucht te zuigen voor brandstoffen en meer?

- Een gemakkelijker recept
 Hoe beweegt warmte -energie in een systeem?
Hoe beweegt warmte -energie in een systeem?  Winst Qantas Airways lager na stijgende olieprijzen
Winst Qantas Airways lager na stijgende olieprijzen Zelfrijdend testvoertuig toegevoegd aan autogeschiedenismuseum
Zelfrijdend testvoertuig toegevoegd aan autogeschiedenismuseum Regels voor het gebruik van getallen in APA Format
Regels voor het gebruik van getallen in APA Format Glasovergang ontmoet Fickiaanse-niet-Gaussiaanse diffusie
Glasovergang ontmoet Fickiaanse-niet-Gaussiaanse diffusie Wat is nanotechnologie?
Wat is nanotechnologie?  Benin ziet videogaming in het spel voor banen en ontwikkeling
Benin ziet videogaming in het spel voor banen en ontwikkeling Lichaamsdelen van een krokodil
Lichaamsdelen van een krokodil
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

