
Wetenschap
Wat is de reactie wanneer ijzer III -acetaat in water wordt gestopt?
1. Oplossing en ionisatie:
* IJzer (III) Acetaat lost op in water en scheidt zich in zijn samenstellende ionen:
Fe (ch 3 COO) 3 (s) → fe
3+
(aq) + 3ch 3 COO
-
(aq)
2. Hydrolyse van ijzer (III) ionen:
* De ijzer (iii) ionen (fe
3+
) reageren met watermoleculen, vormt gehydrateerde ijzer (III) ionen en brengt hydroniumionen vrij (H 3 O
+
):
Fe
3+
(aq) + h 2 O (l) ⇌ [fe (h 2 O) 6 ]
3. Hydrolyse van acetaationen:
* De acetaationen (ch 3 COO
-
) kan ook reageren met water, waardoor azijnzuur wordt gevormd (CH 3 COOH) en hydroxide-ionen (oh
-
):
CH 3 COO
-
(aq) + h 2 O (l) ⇌ CH 3 COOH (aq) + oh
-
(aq)
4. Evenwicht en pH:
* Deze reacties bereiken een evenwicht, resulterend in een enigszins zure oplossing (pH <7) vanwege de aanwezigheid van hydroniumionen.
5. Vorming van neerslag:
* Afhankelijk van de concentratie van ijzer (III) acetaat en de pH van de oplossing, ijzer (III) hydroxide (Fe (OH) 3 ) kan neerslaan als een roodbruine vaste stof.
Samenvatting:
De reactie van ijzer (III) acetaat met water is een complex proces met oplossing, ionisatie, hydrolyse en evenwicht. Het uiteindelijke resultaat hangt af van factoren zoals concentratie en pH. De oplossing zal enigszins zuur zijn en kan een roodbruine neerslag van ijzer (III) hydroxide bevatten.
 Wil je weten wat oude koala's aten? Controleer de tanden van moderne koala's
Wil je weten wat oude koala's aten? Controleer de tanden van moderne koala's  Welk voorbeeld doet Alan met mij en geeft om aan te tonen dat de natuur een beetje bezorgdheid heeft over dingen die je mijn belangrijke verplaatst?
Welk voorbeeld doet Alan met mij en geeft om aan te tonen dat de natuur een beetje bezorgdheid heeft over dingen die je mijn belangrijke verplaatst?  Wat is studie van ontwerp en doel in de natuur?
Wat is studie van ontwerp en doel in de natuur?  Wie ontdekte het licht van licht?
Wie ontdekte het licht van licht?  Waarom rode algen nooit het droge land hebben gekoloniseerd
Waarom rode algen nooit het droge land hebben gekoloniseerd
Hoofdlijnen
- Een DNA -streng bevat de basissequentie AGTT. Wat is complementair DNA?
- Man of vrouw? Wetenschappers ontdekken het genetische mechanisme dat de geslachtsontwikkeling bij vlinders bepaalt
- De meeste bijen sterven niet na steken – en andere verrassende bijenfeiten
- Hoe een opkomende ziekte bij honden licht werpt op cystische fibrose
- Waarom is stamcelbehandeling een wetenschappelijke controverse?
- Wat is glycouse?
- Waarom fruitvliegjes een goed genetisch model zijn voor onderzoek naar ziekten bij de mens
- Onderzoekers ontdekken verschillende levenscyclusfasen van de ectosymbiotische DPANN-archaeon Nanobdella aerobiophila
- De diversiteit aan gewassen ter wereld documenteren en beschikbaar maken
- Tubuline-remmer met een uniek moleculair werkingsmechanisme

- Biologisch geïnspireerd, hoogwaardig polyurethaan ontwikkeld voor rekbare elektronica

- Illinois-onderzoekers theorie van transport op porieschaal om verbeterde stroombatterijen mogelijk te maken

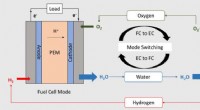
- Nieuwe katalysator helpt brandstofcel te combineren, batterij in één apparaat
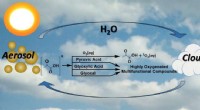
- Organische 2-oxocarbonzuren zorgen voor een link naar de vorming van radicalen en reactieve zuurstofsoorten in atmosferische deeltjes
 Hoe vertegenwoordigen transistoren binair?
Hoe vertegenwoordigen transistoren binair?  Kun je veilig naar een gedeeltelijke zonsverduistering kijken?
Kun je veilig naar een gedeeltelijke zonsverduistering kijken?  Klimaatverandering kan gevaarlijk zijn voor uw gezondheid
Klimaatverandering kan gevaarlijk zijn voor uw gezondheid Papoea-Nieuw-Guinea luiken vervuilen Chinese fabriek
Papoea-Nieuw-Guinea luiken vervuilen Chinese fabriek Welke energie wordt overgedragen bij het verwarmen van water?
Welke energie wordt overgedragen bij het verwarmen van water?  Waarom is het belangrijk voor Cotrol Vaibles in een experiment?
Waarom is het belangrijk voor Cotrol Vaibles in een experiment?  Kan het injecteren van deeltjes in de stratosfeer de opwarming van de aarde vertragen?
Kan het injecteren van deeltjes in de stratosfeer de opwarming van de aarde vertragen?  Hoe beïnvloedt warmte -energie deeltjesbeweging?
Hoe beïnvloedt warmte -energie deeltjesbeweging?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

