
Wetenschap
Is normaliteit en molariteit voor natriumthiosulfaat hetzelfde?
* molariteit vertegenwoordigt het aantal mol opgeloste stof per liter oplossing.
* Normaliteit vertegenwoordigt het aantal equivalenten van opgeloste stof per liter oplossing.
Natriumthiosulfaat (Na₂s₂o₃) heeft twee equivalenten per mol vanwege de aanwezigheid van twee zwavelatomen die redoxreacties kunnen ondergaan.
Daarom is de normaliteit van een natriumthiosulfaatoplossing tweemaal de molariteit.
Voorbeeld:
Een 0,1 M oplossing van natriumthiosulfaat zal een normaliteit hebben van 0,2 N.
Belangrijke opmerking: Normaliteit is geen universele eenheid en hangt af van de specifieke reactie die wordt overwogen. In sommige reacties kan natriumthiosulfaat een ander aantal equivalenten hebben. Het is altijd het beste om de specifieke reactie op te geven bij het gebruik van normaliteit.
 Noem de twee verschillende soorten metallurgie?
Noem de twee verschillende soorten metallurgie?  Wat gebeurt er bij de faseverandering van condensatie?
Wat gebeurt er bij de faseverandering van condensatie?  Bio-ingenieurs zetten stap in de richting van een patch die een gebroken hart kan herstellen
Bio-ingenieurs zetten stap in de richting van een patch die een gebroken hart kan herstellen Hoe supervulkanen werken
Hoe supervulkanen werken  Wat is een voorbeeld van hoe onderzoek naar de effecten die een chemische stof heeft veranderd?
Wat is een voorbeeld van hoe onderzoek naar de effecten die een chemische stof heeft veranderd?
 Atmosferische ijsdeeltjes kleiner en vallen sneller dan modellen hadden aangenomen
Atmosferische ijsdeeltjes kleiner en vallen sneller dan modellen hadden aangenomen Kritisch bedreigde Zuid-Amerikaanse bossen zijn door de mens gemaakt
Kritisch bedreigde Zuid-Amerikaanse bossen zijn door de mens gemaakt Wat we niet weten (over meren) kan ons pijn doen
Wat we niet weten (over meren) kan ons pijn doen Globale analyse van onderzeese canyons kan licht werpen op Marslandschappen
Globale analyse van onderzeese canyons kan licht werpen op Marslandschappen Tropische storm Fay verzwakt na aanlanding New Jersey (update)
Tropische storm Fay verzwakt na aanlanding New Jersey (update)
Hoofdlijnen
- Hoeveel chromosomen zijn er in een dandilion?
- Inheemse vissoorten lopen gevaar na verwijdering van water uit de Colorado-rivier
- Waarom de antilichamen anti A en B in bloedgroep O vernietigen cellen van of vernietigen niet?
- Twee zijden van DNA -ladder zijn losjes aan elkaar verbonden door wat?
- Waar zijn ribosomen op geconstrueerd?
- Waarom natuurlijke netwerken stabieler zijn dan door de mens gemaakte netwerken
- Onderzoekers ontdekken hoe fotosynthetische organismen ATP reguleren en synthetiseren
- Wat anders tussen relatieve en een absolute celreferentie?
- Wat is een bijestinfectie?
- Niet-invasieve diagnose van prostaatkanker, toezicht houden

- Metalen beïnvloeden C-peptidehormoon gerelateerd aan insuline

- Soja-microbeads zijn een milieuvriendelijk alternatief voor plastic microbeads die worden gebruikt in cosmetica, zeep producten

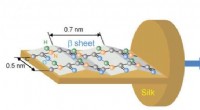
- Nieuwe infraroodbeeldvormingstechniek onthult moleculaire oriëntatie van eiwitten in zijdevezels
- Video:Het Vrijheidsbeeld ware kleuren

 Wat gebeurt er in het lichaam als deeltjes van een plek met veel van hen naar minder gaan?
Wat gebeurt er in het lichaam als deeltjes van een plek met veel van hen naar minder gaan?  Verbetering van de detectie van antilichamen tegen het Afrikaanse varkenspestvirus in serum
Verbetering van de detectie van antilichamen tegen het Afrikaanse varkenspestvirus in serum Onderzoek volgt het gebruik van watervogels in wetlands in de omgeving van Chicago
Onderzoek volgt het gebruik van watervogels in wetlands in de omgeving van Chicago De chaostheorie biedt een manier om te bepalen hoe verontreinigende stoffen zich verplaatsen
De chaostheorie biedt een manier om te bepalen hoe verontreinigende stoffen zich verplaatsen  Blijft het totale aantal atomen hetzelfde tijdens een chemische reactie?
Blijft het totale aantal atomen hetzelfde tijdens een chemische reactie?  Trump belooft Chinese telecombanen veilig te stellen (update)
Trump belooft Chinese telecombanen veilig te stellen (update) Is het waar dat water de neiging heeft om te diffunderen van een gebied waar de droesem geconcentreerd is naar zeer geconcentreerd?
Is het waar dat water de neiging heeft om te diffunderen van een gebied waar de droesem geconcentreerd is naar zeer geconcentreerd?  Hoe is de golfsnelheid en de dichtheid van een bepaald medium gekoppeld?
Hoe is de golfsnelheid en de dichtheid van een bepaald medium gekoppeld?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

