
Wetenschap
Balansvergelijking. Wanneer een waterige oplossing van lood II -nitraat wordt gemengd met natriumjodide en een gele vaste stof wordt gevormd?
De reactie
De reactie die je beschrijft is een neerslagreactie. Wanneer waterige oplossingen van lood (II) nitraat (PB (NO₃) ₂) en natriumjodide (NAI) worden gemengd, een felgele vaste stof, lood (II) jodide (PBI₂), neerslaat uit oplossing.
De evenwichtige vergelijking
`` `
Pb (no₃) ₂ (aq) + 2 nai (aq) → pbi₂ (s) + 2 nano₃ (aq)
`` `
Verklaring van balanceren
* lead (pb): Er is één loodatoom aan elke kant van de vergelijking.
* nitraat (no₃): Er zijn twee nitraationen aan de linkerkant en twee aan de rechterkant.
* natrium (NA): Er zijn twee natriumatomen aan elke kant.
* jodium (i): Er zijn twee jodiumatomen aan elke kant.
Key Points
* (aq) geeft aan dat de stof is opgelost in water (waterige oplossing).
* (s) geeft aan dat de stof een vaste stof is (neerslag).
* Het gevormde gele neerslag is lood (ii) jodide (PBI₂).
* De reactie is gebalanceerd omdat het aantal atomen van elk element hetzelfde is aan beide zijden van de vergelijking.
Waarom de reactie optreedt
Lood (ii) jodide (PBI₂) is zeer onoplosbaar in water. Wanneer de oplossingen worden gemengd, komen de lood- en jodide -ionen samen om een vaste stof te vormen die scheidt van de oplossing. Dit is een klassiek voorbeeld van een dubbele verplaatsingsreactie waarbij de ionen van partners wisselen.
 China waarschuwt voor ernstige oogstdreiging door ergste hittegolf ooit
China waarschuwt voor ernstige oogstdreiging door ergste hittegolf ooit Indonesië verzendt tonnen Australisch afval terug
Indonesië verzendt tonnen Australisch afval terug Onderwaterrobot volgt giftige algen in Lake Erie
Onderwaterrobot volgt giftige algen in Lake Erie Hoe bittere koude winteruitbarstingen en een opwarmende planeet de kustlijn van Lake Michigan zullen opvreten?
Hoe bittere koude winteruitbarstingen en een opwarmende planeet de kustlijn van Lake Michigan zullen opvreten? Hoe absorberen planten water uit de grond?
Hoe absorberen planten water uit de grond?
Hoofdlijnen
- Een fossiele baby hielp wetenschappers uit te leggen hoe zoogdieren floreerden na het uitsterven van de dinosauriërs
- Wat is het genotype van twee zwarte heterozygote cavia?
- Gentherapie biedt langdurige behandeling voor muizen met diabetes
- De vrouwelijke gameten ontwikkelen zich in structuren die follikels worden genoemd. Wat is een follikel?
- Wat is een ander woord dat wetenschappers fouten gebruiken?
- Wat is een geïsoleerd systeem?
- Wat zijn de interacties tussen orgaansystemen?
- Wat is een koolhydraat gevonden in een celwand van plantencellen?
- Waarom sterven sommige subtypes van het griepvirus uit?
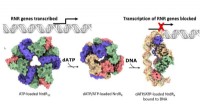
- Nieuw mechanisme voor het reguleren van de aanvoer van DNA-bouwstenen voor betere antibiotica
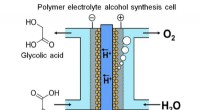
- Onderzoek naar elektrolyse voor energieopslag
- Langetermijnstudie van gelijmde stalen wapeningen op een betonnen balk gaat 50e jaar in

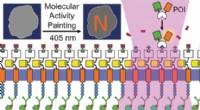
- Molecular activity painting om schakelaarachtige, lichtgestuurde verstoringen in cellen
- Vallen voor energiebronmoleculen in cellen
 Welke heeft meer massa een mol kalium of natrium?
Welke heeft meer massa een mol kalium of natrium?  Landt een ruimtevaartuig op de maan?
Landt een ruimtevaartuig op de maan?  Wat is de term voor effecten van elektriciteit op hout?
Wat is de term voor effecten van elektriciteit op hout?  Wat voor soort klimaat overleven Ticks in?
Wat voor soort klimaat overleven Ticks in?  Wat bevat grondwater van nature waardoor het kalksteen en van grotten kan oplossen?
Wat bevat grondwater van nature waardoor het kalksteen en van grotten kan oplossen?  Verborgen verleden van de oudste continenten van de aarde opgegraven
Verborgen verleden van de oudste continenten van de aarde opgegraven Engelennummer 1111:de betekenis en betekenis ervan ontsluiten
Engelennummer 1111:de betekenis en betekenis ervan ontsluiten  Winst BMW daalt in volatiele tijden
Winst BMW daalt in volatiele tijden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

