
Wetenschap
Wat is de Lewis Dot -structuur voor waterstofsulfide?
1. Bepaal het totale aantal valentie -elektronen:
* Waterstof (H) heeft elk 1 valentie -elektron en er zijn 2 waterstofatomen.
* Zwavel (s) heeft 6 valentie -elektronen.
* Totale valentie -elektronen =(2 x 1) + 6 =8
2. Bepaal het centrale atoom:
* Zwavel is minder elektronegatief dan waterstof, dus het zal het centrale atoom zijn.
3. Verbind de atomen met enkele bindingen:
* Teken twee waterstofatomen verbonden met het zwavelatoom met enkele bindingen. Dit maakt gebruik van 2 van de 8 valentie -elektronen.
4. Verdeel de resterende elektronen:
* Zwavel heeft 6 elektronen nodig om zijn octet te voltooien. Plaats 2 eenzame paren (4 elektronen) rond het zwavelatoom. Dit maakt gebruik van alle 8 valentie -elektronen.
De Lewis Dot -structuur voor H₂s ziet er zo uit:
H
|
S
|
H
Sleutelpunten:
* Het zwavelatoom heeft 2 eenzame paren elektronen.
* Elk waterstofatoom heeft 1 binding en vervult zijn duetregel.
* Het zwavelatoom heeft in totaal 8 elektronen (2 obligaties + 4 eenzame paar elektronen) en vervult zijn octetregel.
Hoofdlijnen
- Leg de rol van een hypothese uit bij wetenschappelijk onderzoek?
- Levens in evenwicht:waarom houden we vast aan potentieel schadelijke, ziekteverwekkende mutaties?
- Wat gebeurt er met de bacteriën als het wordt gemengd met witte bloedcellen?
- Een computerinstrument voorspelt hoe het darmmicrobioom in de loop van de tijd verandert
- Hoe een Silly Putty-ingrediënt stamceltherapieën zou kunnen bevorderen
- Waarom wiebelen planten? Nieuw onderzoek biedt antwoorden
- Waar worden de chromosomen voor het eerst?
- Is creatinekinase oplosbaar in water?
- De code van colibactine kraken:onderzoek onderzoekt hoe de verbinding het DNA beschadigde om het verband met kanker te begrijpen
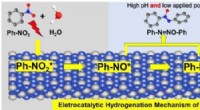
- Hydrogeneringsregeling van nitrobenzeen in elektrokatalytische processen gerealiseerd
- Onderzoekers rapporteren nieuwe klasse polyethyleenkatalysator

- Ultraheldere röntgenstralen onthullen de moleculaire structuur van membranen die worden gebruikt om zeewater te ontzilten

- Met een meerlagige aanpak, een filter om te voldoen aan de behoeften van de zoetwatervoorziening

- Eersteklas YEATS-remmers die veelbelovend zijn voor de behandeling van leukemie

 Onderzoek naar de deeltjesgrootte en depositie van dampen
Onderzoek naar de deeltjesgrootte en depositie van dampen Hoe is de kracht gerelateerd aan het product van twee ladingen?
Hoe is de kracht gerelateerd aan het product van twee ladingen?  Sommige lemuren zijn eenlingen, anderen hunkeren naar verbinding
Sommige lemuren zijn eenlingen, anderen hunkeren naar verbinding Klimaatverandering heeft miljarden dollars aan schade veroorzaakt door overstromingen
Klimaatverandering heeft miljarden dollars aan schade veroorzaakt door overstromingen Cruciale nieuwe gegevens over de oorsprong van de hunebedden van Antequera, een Werelderfgoed
Cruciale nieuwe gegevens over de oorsprong van de hunebedden van Antequera, een Werelderfgoed Wat is de productie en overdracht van stralende energie?
Wat is de productie en overdracht van stralende energie?  Welk type sporen produceren lycopodium?
Welk type sporen produceren lycopodium?  Verborgen rivier stroomde ooit onder Antarctisch ijs
Verborgen rivier stroomde ooit onder Antarctisch ijs
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


