
Wetenschap
Een verbinding gevormd uit alleen fosfor en zuurstof blijkt 56.35 te zijn wat de empirische formule -verbinding?
1. Ga uit van een 100 g monster
* Dit maakt de berekeningen eenvoudiger. Als de verbinding 56,35% fosfor is, dan is deze ook 56,35 g fosfor in een 100 g monster.
* Het resterende percentage (100% - 56,35% =43,65%) is zuurstof, of 43,65 g zuurstof in het monster.
2. Converteer grams naar mollen
* Gebruik de molaire massa van elk element om grammen om te zetten in mollen:
* Fosfor (p):56,35 g / 30,97 g / mol ≈ 1,82 mol
* Zuurstof (O):43,65 g / 16,00 g / mol ≈ 2,73 mol
3. Zoek de eenvoudigste molratio
* Verdeel elke molwaarde door de kleinste molwaarde:
* Fosfor:1,82 mol / 1.82 mol ≈ 1
* Zuurstof:2,73 mol / 1,82 mol ≈ 1,5
4. Aanpassen aan hele getallen
* Aangezien we een 1,5 -verhouding voor zuurstof hebben, vermenigvuldig beide verhoudingen met 2 om hele getallen te krijgen:
* Fosfor:1 * 2 =2
* Zuurstof:1.5 * 2 =3
5. Schrijf de empirische formule
* De empirische formule vertegenwoordigt de eenvoudigste verhouding van het hele nummer van atomen in de verbinding.
* De empirische formule is p₂o₃ .
 Nieuwe strategie om katalysatoren met één atoom te fabriceren via elektrochemische depositie
Nieuwe strategie om katalysatoren met één atoom te fabriceren via elektrochemische depositie Van welke elementen bestaat kopernitraat?
Van welke elementen bestaat kopernitraat?  Hoeveel moleculen natrium en kalium worden in welke richting verplaatst?
Hoeveel moleculen natrium en kalium worden in welke richting verplaatst?  Universele pH-gereguleerde assemblage van DNA-nanostructuren
Universele pH-gereguleerde assemblage van DNA-nanostructuren Welk materiaal is niet ontvlambaar?
Welk materiaal is niet ontvlambaar?
 NASA-studie vindt dat het vermogen van tropische bossen om koolstofdioxide te absorberen afneemt
NASA-studie vindt dat het vermogen van tropische bossen om koolstofdioxide te absorberen afneemt Verwanten van de Zebra
Verwanten van de Zebra Landbouw vervangt fossiele brandstoffen als grootste menselijke bron van zwavel voor het milieu
Landbouw vervangt fossiele brandstoffen als grootste menselijke bron van zwavel voor het milieu Studie toont universeel positief effect van bodembedekkers op bodemmicrobioom
Studie toont universeel positief effect van bodembedekkers op bodemmicrobioom Schone energienetwerken en elektrische voertuigen essentieel om klimaatverandering en luchtvervuiling te verslaan
Schone energienetwerken en elektrische voertuigen essentieel om klimaatverandering en luchtvervuiling te verslaan
Hoofdlijnen
- Hoe kan de grootte van een molecuul de manier beïnvloeden waarop een organisme voedingsstoffen verkrijgt die moleculen?
- Door licht geactiveerd antitumormedicijn zou nieuwe kankerbehandelingen kunnen inspireren die minimale bijwerkingen hebben
- Wat is wetenschappelijke naam?
- Lijst met schimmelvoordelen
- Wat stelt mensen in staat om verschillende eigenschappen te hebben?
- Apen die onder druk staan tonen hun vindingrijkheid – en verwijzen naar ons eigen evolutionaire verleden
- Hoe een menselijke cel te maken voor een wetenschapsproject
- Volgens Lamarck evolueerde soorten?
- Nieuwe functies voor 'junk'-DNA?
- DNA-schade veroorzaakt door migrerende lichtenergie

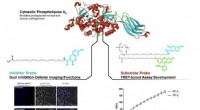
- Fluorescerende sondes om cellulaire activiteit te bestuderen
- Experimentele studie van hoe metallisch glas een uitdaging vormt voor het paradigma in glasonderzoek

- Metaalionkatalysatoren en waterstofperoxide kunnen de plasticproductie groener maken

- Nieuwe hydrogels zijn veelbelovend bij de behandeling van botdefecten
 Welk deel van de energie is verantwoordelijk voor het drogen van kleding?
Welk deel van de energie is verantwoordelijk voor het drogen van kleding?  Waarom hebben vloeistoffen en gassen geen moduli?
Waarom hebben vloeistoffen en gassen geen moduli?  Natuurkundigen observeren voor het eerst individuele atoombotsingen tijdens diffusie
Natuurkundigen observeren voor het eerst individuele atoombotsingen tijdens diffusie Nieuw onderzoek laat zien hoe koolzuurhoudend water kan worden gebruikt om de eigenschappen van hydrogels voor verschillende toepassingen af te stemmen
Nieuw onderzoek laat zien hoe koolzuurhoudend water kan worden gebruikt om de eigenschappen van hydrogels voor verschillende toepassingen af te stemmen  Mediterrane potvissen vertonen grote variaties in grootte
Mediterrane potvissen vertonen grote variaties in grootte  Klei op Antarctica van miljoenen jaren geleden onthult klimaatveranderingen uit het verleden
Klei op Antarctica van miljoenen jaren geleden onthult klimaatveranderingen uit het verleden Waarom zie je ringen van de aarde?
Waarom zie je ringen van de aarde?  Online wetenschappelijke en wiskundige bronnen voor leerkrachten van jonge kinderen
Online wetenschappelijke en wiskundige bronnen voor leerkrachten van jonge kinderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

