
Wetenschap
Wat is de reactie van fosforzuur met trisodiumfosfaat?
Hier is de evenwichtige chemische vergelijking:
h₃po₄ (aq) + 2na₃po₄ (aq) → 3na₂hpo₄ (aq) + nah₂po₄ (aq)
Verklaring:
* Fosforzuur (H₃po₄) is een triprotisch zuur, wat betekent dat het drie protonen kan doneren (H+).
* Trisodiumfosfaat (Na₃po₄) is een sterke basis.
* De reactie omvat de overdracht van protonen van het zuur naar de basis.
De reactie kan worden verklaard in stappen:
1. Eerste protonoverdracht: H₃po₄ reageert met na₃po₄ om na₂hpo₄ en nah₂po₄ te vormen.
2. Tweede protonoverdracht: H₃po₄ reageert met een ander molecuul van Na₃po₄ om een ander molecuul van Na₂hpo₄ te vormen.
3. Derde protonenoverdracht: De resterende H₃po₄ reageert met het laatste molecuul van Na₃po₄ om een ander molecuul na₂hpo₄ en een molecuul nah₂po₄ te vormen.
Over het algemeen resulteert de reactie in de vorming van dinatriumwaterstoffosfaat (Na₂hpo₄) en natriumdihydrogen fosfaat (NAH₂PO₄) in een molaire verhouding van 3:1.
Opmerking: Deze reactie is sterk afhankelijk van de stoichiometrie van de reactanten. Als er een teveel aan fosforzuur is, zullen de eindproducten anders zijn.
 Wat is de chemische formule voor N3-?
Wat is de chemische formule voor N3-?  Hoe het aantal representatieve deeltjes in elke stof te vinden
Hoe het aantal representatieve deeltjes in elke stof te vinden Waarom werkt de geleiding goed in vloeistoffen maar werkt echt vaste stoffen?
Waarom werkt de geleiding goed in vloeistoffen maar werkt echt vaste stoffen?  Onderzoekers gebruiken Theta voor realtime analyse van COVID-19-eiwitten
Onderzoekers gebruiken Theta voor realtime analyse van COVID-19-eiwitten Acetal wordt gebruikt bij de productie van welke montage?
Acetal wordt gebruikt bij de productie van welke montage?
 Hoe is het Ecosysteem van het Northern Lights Effet -ecosysteem?
Hoe is het Ecosysteem van het Northern Lights Effet -ecosysteem?  NASA ziet windschering nog steeds teisteren tropische storm Iselle
NASA ziet windschering nog steeds teisteren tropische storm Iselle Studie beoordeelt bombturbatie en andere langetermijneffecten van explosieve munitie uit de Eerste Wereldoorlog op de bodem
Studie beoordeelt bombturbatie en andere langetermijneffecten van explosieve munitie uit de Eerste Wereldoorlog op de bodem Hoe landverontreiniging te voorkomen
Hoe landverontreiniging te voorkomen Waarom maken bomen krakende geluiden?
Waarom maken bomen krakende geluiden?
Hoofdlijnen
- Hoe zou zout Gist beïnvloeden?
- In de biologie waar voedsel wordt verteerd het eten?
- Orka's migreren, studievondsten, maar waarom?
- Hoe noem je een cel zonder membraan?
- Wat is het doel van een eukaryotische cel?
- Hoe de kern vormt een pollenkorrel die een vrouwelijke eiercel bemoeilijkt?
- Wat werd het raster gebruikt om overervingpatronen op basis van genotype -ouders die werden genoemd?
- Moet het houden van reptielen en amfibieën als huisdier worden beperkt?
- Nieuwe studie voorspelt wereldwijde verandering in ondiepe rifecosystemen als het water warmer wordt
- Onderzoekers komen dichter bij auto's op waterstof
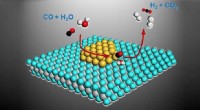
- Wetenschappers ontwikkelen een goedkopere methode die kan helpen bij het maken van brandstoffen uit planten

- Nieuw materiaal biedt milieuvriendelijke oplossing om restwarmte om te zetten in energie

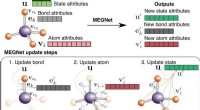
- Ingenieurs gebruiken grafieknetwerken om eigenschappen van moleculen en kristallen nauwkeurig te voorspellen
- Onderzoekers reconstrueren de biochemische mechanismen van fotosynthese

 Freeports:innovatieve handelshubs of centra voor witwassen en belastingontduiking?
Freeports:innovatieve handelshubs of centra voor witwassen en belastingontduiking? NASA-satelliet ziet branden in het zuidoosten van de VS
NASA-satelliet ziet branden in het zuidoosten van de VS Wat weten wetenschappers nu dat hitte is?
Wat weten wetenschappers nu dat hitte is?  Gepersonaliseerde kankervaccins:doorbraak kan betere resultaten opleveren
Gepersonaliseerde kankervaccins:doorbraak kan betere resultaten opleveren Wat is de temperatuur van Barnards -ster?
Wat is de temperatuur van Barnards -ster?  Herinnerend aan Michael Collins,
Herinnerend aan Michael Collins,  Fukushima:Waarom we duizenden jaren terug moeten kijken om beter te worden in het voorspellen van aardbevingen
Fukushima:Waarom we duizenden jaren terug moeten kijken om beter te worden in het voorspellen van aardbevingen Wanneer landden ons voor het eerst op de maan?
Wanneer landden ons voor het eerst op de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

