
Wetenschap
Wat is kaliumhydroxide of natriumhydroxide?
overeenkomsten:
* Sterke bases: Ze dissociëren gemakkelijk in water, brengen hydroxide-ionen (OH-) uit en maken de oplossing zeer alkalisch.
* zeer reactief: Ze reageren krachtig met zuren en produceren warmte en zout.
* corrosief: Ze kunnen ernstige brandwonden voor huid en ogen veroorzaken.
Verschillen:
* chemische formule: KOH heeft kalium (K) terwijl NaOH natrium heeft (NA).
* Oplosbaarheid: NaOH is meer oplosbaar in water dan KOH.
* Toepassingen:
* NaOH: Gebruikt bij het maken van zeep, papierproductie, waterbehandeling en als afvoerreiniger.
* KOH: Gebruikt bij de productie van meststoffen, batterijen en als een reagens in organische synthese.
Key Properties:
| Eigenschap | KOH | NaOH |
| --- | --- | --- |
| Uiterlijk | Wit solide | Wit solide |
| Molecuulgewicht | 56.11 g/mol | 40,00 g/mol |
| Smeltpunt | 360 ° C | 318 ° C |
| Kookpunt | 1327 ° C | 1388 ° C |
| Oplosbaarheid in water | Zeer oplosbaar | Zeer oplosbaar |
| pH | 14 (verzadigde oplossing) | 14 (verzadigde oplossing) |
Veiligheidsmaatregelen:
* altijd met extreme zorg.
* Draag geschikte persoonlijke beschermingsmiddelen (PBM) inclusief handschoenen, bril en laboratoriumjas.
* Bewaar op een koele, droge plaats weg van vocht en onverenigbare stoffen.
* Spoel in geval van contact onmiddellijk het getroffen gebied met veel water en zoek medische aandacht.
Opmerking: Hoewel beide sterke bases zijn, zijn ze niet uitwisselbaar in alle toepassingen. De specifieke eigenschappen van elk zijn belangrijk voor hun beoogde gebruik.
 Ida:uitroepteken op record aanval van Amerikaanse aanlandingen
Ida:uitroepteken op record aanval van Amerikaanse aanlandingen Orkaan Alfa? Verhoogde seizoensvoorspelling, namen kunnen opraken
Orkaan Alfa? Verhoogde seizoensvoorspelling, namen kunnen opraken Oesterjagers verkennen rivieren op tekenen van schelpdierleven
Oesterjagers verkennen rivieren op tekenen van schelpdierleven Voormalig VN-leider bezoekt klimaatadaptatieprojecten in Miami
Voormalig VN-leider bezoekt klimaatadaptatieprojecten in Miami Over hoe het ecologisch evenwicht in detail te behouden?
Over hoe het ecologisch evenwicht in detail te behouden?
Hoofdlijnen
- Zijn prokaryotische cellen het type waaruit planten en dieren vormen?
- Sociale vaardigheden van honden gekoppeld aan gevoeligheid voor oxytocine
- Een methode die wordt gebruikt om de genomen van verschillende organismen of individuen te vergelijken?
- Wat is de functie van borstelreiniger in het laboratorium?
- Molecuul dat een aminozuur naar het ribosoom draagt voor opname in een eiwit?
- Hoe het eerste katachtige sabeltandroofdier werd ontdekt en waarom het verschilt van moderne katten
- Wat is de naam van een groep anders weefsel dat samenwerkt?
- Welk molecuul wordt gebruikt tijdens aerobe ademhaling?
- Amerikaanse restaurateur lost 60 miljoen jaar oude dinosaurusfossielenpuzzels op
- Iridium en 2-methylfenantroline versnellen katalytische boryleringsreacties

- Close-up van groeiende polymeerketen Toon sprongstappen
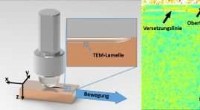
- Materiaalonderzoekers bestuderen de oorzaken van slijtage - permanente moleculaire modificaties treden op bij het eerste contact
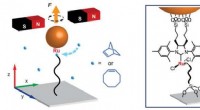
- Lichtgevende organische moleculen bewerken via oppervlaktemodificatie
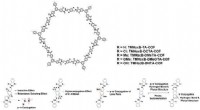
- Nieuw materiaal kan tijd en geld besparen bij medische beeldvorming en milieusanering

 Schedels die wild zijn geworden:hoe en waarom sommige kikkers extreme hoofden ontwikkelden
Schedels die wild zijn geworden:hoe en waarom sommige kikkers extreme hoofden ontwikkelden  Razendsnelle algoritmen kunnen de belasting van het genereren van 3D-hologrammen verlichten
Razendsnelle algoritmen kunnen de belasting van het genereren van 3D-hologrammen verlichten Welk orgaan vernietigt oude rode cellen en slaat witte bloedcellen op?
Welk orgaan vernietigt oude rode cellen en slaat witte bloedcellen op?  Sonaronderzoek toont krater gemaakt door A-bomtest op het Bikini-atol onder water
Sonaronderzoek toont krater gemaakt door A-bomtest op het Bikini-atol onder water Doet technologische toepassingen vaak per ongeluk voor?
Doet technologische toepassingen vaak per ongeluk voor?  Waterveiligheid aanscherpen door regenwateropvang
Waterveiligheid aanscherpen door regenwateropvang Welk type condensatiekernen veroorzaken het meest waarschijnlijk wolkenvorming?
Welk type condensatiekernen veroorzaken het meest waarschijnlijk wolkenvorming?  Zilveren nanodeeltjes eiwit corona beïnvloedt hun toxiciteit
Zilveren nanodeeltjes eiwit corona beïnvloedt hun toxiciteit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

